


���� ��������衿���ݼ���1��2�����ƶϼ���3Ϊ����ʯ�к�+2��+3������
�������о�����1������ʵ�鲽��ڼ�����������Һ��ɫ֤�������������ӣ�
���������
��2��B�еļ�ʯ���������û���Ӧ���ɵ�ˮ�ģ�Ϊ�˷�ֹ�����ɷֶ�ʵ���Ӱ�죬Ҫ��һ��װ�����տ����е�ˮ�Լ�������̼��
��3������װ��D��ˮ�������������Ԫ���غ���㺬��Ԫ���������õ�����ʯ�����İٷֺ�����
��4��һ����̼�ж������ŷſ����У�����H2����CO�����貹��β������װ�ã�
��5����п��Խ�ˮ�е�������ܣ�����ϡ��Һ�������һ���������Һ��ѡ����������ش�
��6������Ԫ���غ�ͻ�ѧ��Ӧ����ʽ���м��㣻������Ԫ��������������Ԫ�������������������������Ļ�ѧʽ��
��� �⣺��������衿����1������ʯ��ֻ��+3����������2������ʯ��ֻ��+2���������ݼ���1��2�������Ԫ�ش��ڵĻ��ϼۣ������ƶϼ���3Ϊ����ʯ�к�+2��+3������
�ʴ�Ϊ������ʯ�к�+2��+3������
�������о�����1������ʵ�鲽��ڣ���ڶ�����Һ�еμ��������������Һ����ǿ�����ԣ�������������Һ��ɫ֤������ԭ��֤�������������ӣ�
�ʴ�Ϊ���ڣ�
���������
��2����ʵ���У���������������Ӧ���ɽ�������ˮ�����ݹ��������ı仯���������ĺ�����B���ĸ�������������ղ�����ˮ����������Cװ��Ҫ��ֹ��ֹ�����е�ˮ������CO2����B�У�Ӱ��ⶨ�����
�ʴ�Ϊ����ֹ�����е�ˮ������CO2����B�У�Ӱ��ⶨ�����
��3������ˮ���������㺬��Ԫ�������õ�����ʯ�����İٷֺ�������ķ�Ӧ��װ��D����1.35g�����ݷ�Ӧ��ʵ�ʣ����ӵ���ˮ�����������������غ㶨�ɣ���������ʯ�����İٷֺ����ǣ�$\frac{\frac{1.35g}{18g/mol}��16g/mol}{5.0g}$��100%=24%��
�ʴ�Ϊ��24%��
��4��һ����̼�ж������ŷſ����У�����H2����CO�����貹��β������װ�ã�
�ʴ�Ϊ��β�����գ�
��5��������ʯ�м������ᣬ����Ӧ���������������Һ�������ڹ�����������Һ�������������������к���Խ����������ܽ�ȣ�������Һ���ܽ�Ĺ�����Cl2����ԭ��Һϡ�͵�250mL����Ҫʹ�õIJ������������У��ձ�������������ͷ�ιܡ�250mL����ƿ����ȱ��250mL����ƿ��
�ʴ�Ϊ��������Һ���ܽ�Ĺ�����Cl2��250mL����ƿ��
��6�����ݷ�Ӧ�ķ���ʽΪ2Fe3++2I-=2Fe2++I2��֪�����ĵĵ����������������ʵ�����ȣ�n��Fe3+��=n��KI��������0.5000mol•L-1��0.020L=c��Fe3+����0.02L�����c��Fe3+��=0.5mol•L-1��������Ԫ�صİٷֺ���Ϊ��$\frac{0.5000mol/L��0.250L��56g/mol}{10.0g}$��100%=70%��
��������������70%����Ԫ�ص�����������24%������100g����ʯ�У���Ԫ�ص�������70g����Ԫ��������24g����Ԫ�غ���Ԫ�ص����ʵ�����Ϊ��$\frac{70}{56}$��$\frac{24}{16}$=5��6��
����������Ļ�ѧʽΪFe5O6��
�ʴ��ǣ�70%��Fe5O6 ��
���� ���⿼����̽������ʯ����Ԫ�غ���Ԫ�صĺ����ķ����������Ǹ߿��еij������ͣ������е��Ѷȵ����⣬���ض�ѧ��������������ѵ��������������ѧ���淶�Ͻ���ʵ����ơ��������������������ۺ���ǿ�����ۺ�ʵ������ϵ���ܣ�Ҫ��ѧ���������桢ϸ�µ����⣬��ϵ��ѧ����֪ʶ�ͼ��ܣ�ȫ��ϸ�µ�˼�����ܵó���ȷ�Ľ��ۣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3+HNO3��NaHCO3+HNO3 | B�� | CaCl2+Na2CO3��Ca��NO3��2+K2CO3 | ||
| C�� | Ba��OH��2+NaHSO4��BaCl2+NaHSO4 | D�� | NaOH+H2SO4��Fe��OH��3+H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õιܵμ�Һ��ʱ���ι�Ӧ�����������Ϸ������ܴ��������ڱ� | |
| B�� | ��ҩ����ֽ�۰ѷ�ĩ״ҩƷ�����Թܵĵײ� | |
| C�� | ����������Һʱ����������Ͳ�м���һ�������ˮ�����ڽ�����������������Ũ���� | |
| D�� | ����ʱ��������ĩ��Ӧ������������ֽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| B�� | �Ȼ�����Һ������Ӧ��Fe3++Fe�T2Fe2+ | |
| C�� | ����������ϡ���ᷴӦ��FeO+2H+�TFe3++H2O | |
| D�� | �Ȼ�����Һ��ͭ��Ӧ��2Fe3++Cu�T2Fe2++Cu2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
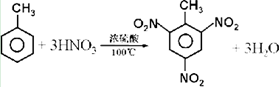 ��
��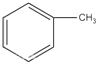 +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$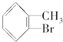 +HBr��
+HBr�� +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$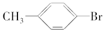 +HBr��
+HBr���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ������̼��������Һ�м�����������ʯ��ˮ HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| B�� | Ư�۵�ϡ��Һ��ͨ�����SO2���� Ca2++2ClO-+SO2+H2O�TCaSO3��+2HClO | |
| C�� | ��֪����ƽ�ⳣ����H2CO3��HClO��HCO3-����NaClO��Һ��ͨ������������̼��2ClO-+CO2+H2O�T2HClO+CO32- | |
| D�� | Ba��OH��2��Һ�������NaHSO4��Һ�У�H++SO42-+Ba2++OH-�TBaSO4��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 30 | B�� | 44 | C�� | 46 | D�� | 80 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com