
����Ŀ��Ϊ̽����������Է�Ӧ��mA(g)+nB(g)![]() cZ(g) ��H��Ӱ�죬��A��B���ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ��������ͼ��ʾ�������ж���ȷ����
cZ(g) ��H��Ӱ�죬��A��B���ʵ���֮��Ϊm��n��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ��������ͼ��ʾ�������ж���ȷ����
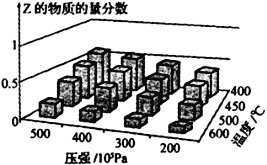
A. �ں��º�ѹ�����£����Ѵﵽƽ�����ϵ�м�������Z������ƽ��ʱ��Z�����ʵ�����������
B. �����¶ȣ������淴Ӧ���ʶ�����ƽ�ⳣ������
C. �¶Ȳ��䣬��Сѹǿ��ƽ�������ƶ�������ƽ��ʱ��A��Ũ�ȱ�ԭƽ���С
D. ��H��0��m+n��c
���𰸡�C
����������ͼ���֪�������¶ȣ�Z�����ʵ�����������˵�������¶�ƽ��������Ӧ�����ƶ�����������Ӧ�Ƿ��ȵģ�����H��0��A���ں��º�ѹ�����£����Ѵﵽƽ�����ϵ�м�������Z��Ϊ����ѹǿ�����������Ϊ��Чƽ�⣬���ﵽ��ͬƽ��״̬��Z�ĺ������䣬A����B�������¶����淴Ӧ���ʶ��ӿ죬��������Ӧ�Ƿ��ȷ�Ӧ������ƽ�ⳣ����С��B����C. ��C֪����H��0 m+n��c���¶Ȳ��䣬����ѹǿ�������С��ƽ�������ƶ�������ƽ��ʱ������ı�����Ҫ���ã�����A��Ũ�ȱ�ԭƽ������C��ȷ��D������Ӧ�Ƿ��ȵģ�����H��0����Сѹǿ����ѧƽ������������ϵ�������ӵķ�����еģ�������m+n��c��D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ�������
�ٱ�״���£�0.2 mol�κ����ʵ������Ϊ4.48 L������1 mol��������Ϊ22.4 L������һ�����ڱ�״���¡��۱�״���£�1 L HCl��1 L H2O�����ʵ�����ͬ���ܱ�״���£�1 g H2��14 g N2�������ͬ����28 g CO�����Ϊ22.4 L�����������ʵ����ʵ�����ͬ���������ڱ�״���µ����Ҳ��ͬ������ͬ��ͬ���ʱ���������ʵ����ʵ���Խ����ѹǿԽ��ͬ��ͬѹ�£�������ܶ����������Է�������������
A. �٢ڢۢ� B. �ڢۢޢߢ� C. �ݢޢߢ� D. �ܢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaBH4/H2O2ȼ�ϵ��(DBFC)�Ľṹ��ͼ��ʾ���õ���ܷ�Ӧ����ʽ��NaBH4 +4H2O2=NaBO2 +6H2O���йص�˵������ȷ����

A. ����MnO2������������ԭ��صĹ���Ч��
B. �ŵ�����У�Na+��B��������A����
C. ��ظ����ĵ缫��ӦΪ��BH4 +8OH- - 8eһ =BO2-+6H2O
D. �ڵ�ط�Ӧ�У�ÿ����1L 1mol��L H2O2��Һ��������������·�еĵ���Ϊ2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�����ڹ�ũҵ����������Ҫ�����á�
��1����֪����C(s)+O2(g)=CO2(g) ��H1=-393.5kJ/mol��
��C(s)+CO2(g)=2CO(g) ��H2=+172.5kJ/mol
��4Fe(s)+3O2(g)=2Fe2O3(s) ��H3=-1651.0kJ/mol
CO��ԭFe2O3���Ȼ�ѧ����ʽΪ__________________________________________��
��2����¯���������ĸ�¯���к���CO��H2��CO2�����壬��CO��H2�ڴ��������ºϳɼ״����Ǽ�����Ⱦ����Լ��Դ���¾ٴ룬��Ӧԭ����CO(g)+2H2(g)![]() CH3OH(g) ��H���������ͬ�����������ܱ������зֱ����1molCO��2mol H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��
CH3OH(g) ��H���������ͬ�����������ܱ������зֱ����1molCO��2mol H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��

������ͼA��B��C�����У�ѡ����Ӧ�±���������С�ĵ㡣
��Ӧ���� | ƽ�ⳣ��K | ƽ��ת������ |
_________ | _________ | _________ |
����300��ʱ����C��ƽ����ϵ���ٳ���0. 5molCO��1.0molH2��0.5mol��CH3OH���÷�Ӧ��_________������У���������Ӧ�������淴Ӧ���������ƶ�������
��һ���¶��£�CO��ת��������ʼͶ�ϱ�[n(H2)/n(CO)]�ı仯��ϵͼ��ʾ�����D��������ת����Ϊ40%����x=_____________��

��3�����Ȼ�����һ����Ҫ�Ļ��������������ʴ��·�塣ij��ʴ��Һ�к���0.5mol��L-1Fe3+��0.26mol��L-1��Cu2+����ʹFe3+��ȫ����[c(Fe3+)��4��l0-5]��Cu2+�����������������ҺpH�ķ�ΧΪ_________��[KspCu(OH)2=2.6��l0-19��KspFe(OH)3=4��l0-38]
��4��Ī���Σ�����ˮ����������茶��壬��һ����Ҫ�Ļ���ԭ�ϣ��ڿ����л����绯����������֤��һƿ���õ�Ī�����Ѿ�������������Ҫ����ʵ������ǣ�ȡ������Ʒ��������ˮ�ܽ⣬����Һ�ֳ����ݣ�______________________________________����֤������Ʒ�Ѳ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��RΪԭ�������������������Ԫ�أ�λ��Ԫ�����ڱ���ǰ�����ڡ�BԪ��ԭ�Ӻ���3���ܼ����Қ����ܼ������ĵ�������ͬ��D��ԭ�Ӻ�����8���˶�״̬��ͬ�ĵ��ӣ�EԪ����FԪ�ش���ͬһ�������ڵ��壬���ǵ�ԭ���������3����EԪ�صĻ�̬ԭ��3d�������4��δ�ɶԵ��ӡ���ش��������⣺
��1��д��C��̬ԭ�ӵļ۲�����Ų�____________��F��̬ԭ�ӵ���Χ�����Ų�ʽ_____________��
��2������˵������ȷ����____________ (����ţ���
A�������������Է��������ȶ�����̼�����Էе㣺SiO2 > CO2
B����һ��������С�����˳��B <C < D
C��N2��COΪ�ȵ����壬�ṹ����
D���ȶ��ԣ�H2O> H2S��ˮ���Ӹ��ȶ���ԭ����ˮ���Ӽ�������
��3��FԪ��λ�����ڱ���_________�����������������ڶ���ø�ĸ����ӣ��˹�ģ��ø�ǵ�ǰ�о����ȵ㡣��F����������Һ��ͨ�˹�����C��A�γɵ�����X������[F(X)4]2+�������ӵĽṹʽΪ__________(��Ԫ�ط��ű�ʾ����
��4��ij��������F(I)��I��ʾ���ϼ�Ϊ+ 1)����γ���ͼ1��ʾ�����ӣ���������̼ԭ�ӵ��ӻ���ʽΪ________________________________��
��5��B���ʵ�һ��ͬ��������ľ�������ͼ2��ʾ����һ������������Bԭ�ӵĸ���Ϊ____________��

��6��D��F�γ����Ӹ�����Ϊ1��1�Ļ�����,������NaCl���ƣ���D���ӵİ뾶Ϊapm�� F���ӵİ뾶bpm����þ����Ŀռ�������Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ��ʵ���ǣ�
A.������ʧ��B.���ϼ۵�����
C.��������������D.���ӵĵ�ʧ��ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�������������������ɣ���ṹʾ��ͼ���£���������S��S����Ϊ��������һSH�����ɵĶ���������������������������������õ����ʷ��ӹ���A����������ɣ����γ�һ���õ����ʷ���ʱ���ٵ���Է�������Ϊ:

A. 18��A��3��+4 B. 18��A��2��+4
C. 18m��A��3�� D. 18��A��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B�ֱ�Ϊ0.6 mol��0.5 mol����0.4 L�ܱ������з�����Ӧ��3A��B![]() aC��2D����5 min��ʱCΪ0.2 mol����֪�ڴ˷�Ӧʱ���ڣ�D��ƽ����Ӧ����Ϊ0.1 mol��(L��min)��1�����н�����ȷ����(����)
aC��2D����5 min��ʱCΪ0.2 mol����֪�ڴ˷�Ӧʱ���ڣ�D��ƽ����Ӧ����Ϊ0.1 mol��(L��min)��1�����н�����ȷ����(����)
A. ��ʱ����Ӧ������ܵ����ʵ���Ϊ1 mol B. B��ת����Ϊ50%
C. A��ƽ����Ӧ����Ϊ0.1 mol��L��1��min��1 D. aֵΪ2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����������������������ȷ����( )
A. ��״���£�22.4L H2O���еķ�����Ϊ NA
B. ͨ��״���£�NA ��CO2����ռ�е����Ϊ22.4L
C. ���ʵ���Ũ��Ϊ1mol/L��MgCl2��Һ�У�����Cl������Ϊ2NA
D. ���³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com