
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
 |  |  | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A. | 装置甲中的A处发生了还原反应 | B. | 装置乙中的C金属是负极 | ||
| C. | 装置丙中的D金属是原电池的正极 | D. | 四种金属的活泼性顺序是D>A>B>C |
分析 甲、乙、丙为原电池装置,甲中A不断溶解,说明A被氧化,为原电池负极,B为正极,乙中C的质量增加,说明C极上析出金属,为原电池正极,则B为负极,丙中A上有气体产生,应为氢气,说明A为正极,则D为负极,原电池反应中负极较活泼,以此解答该题.
解答 解:甲、乙、丙为原电池装置,甲中A不断溶解,说明A被氧化,为原电池负极,B为正极,乙中C的质量增加,说明C极上析出金属,为原电池正极,则B为负极,丙中A上有气体产生,应为氢气,说明A为正极,则D为负极,原电池反应中负极较活泼,则金属的活泼性顺序为D>A>B>C,
A.甲中A不断溶解,说明A被氧化,A处发生了氧化反应,故A错误;
B.乙中C的质量增加,说明C极上析出金属,C为原电池正极,故B错误;
C.丙中A上有气体产生,应为氢气,说明A为正极,则D为负极,故C错误;
D.由以上分析可知金属的活泼性顺序为D>A>B>C,故D正确.
故选D.
点评 本题考查了原电池原理,侧重于金属的活泼性的考查,注意根据原电池电极上得失电子来判断正负极,一般来说,作原电池负极的金属金属活动性顺序强,难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:选择题
| A. | 总质量一定的油脂,无论以何种比例组合,完全水解后生成甘油的量不变 | |
| B. | 用甘氨酸(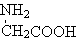 )和丙氨酸( )和丙氨酸( )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 | |
| C. | 用碳酸钠溶液不能区分乙醇、乙酸、苯和硝基苯四种有机物 | |
| D. | 苯酚和苯甲醇互为同系物,均能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) | |
| B. | 常温下,pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) | |
| C. | 0.1 mol•L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| D. | 0.1 mol•L-1的硫化钠溶液中:c(OH-)+c(HS-)+c(S2-)=c(H+)+c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOCH2CH2COOH | B. | HOOC-COOH | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 向100mL 3mol/L的NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.
向100mL 3mol/L的NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别乙醇、苯和溴苯 | |
| B. | 用酸性高锰酸钾溶液鉴别苯、已烯、己烷 | |
| C. | 用饱和碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用燃烧法鉴别乙醇、苯和四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知该分子中含有四面体结构的碳原子数为a,可在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )
已知该分子中含有四面体结构的碳原子数为a,可在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )| A. | 2、3、5 | B. | 3、3、6 | C. | 2、5、4 | D. | 4、6、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 组别 | 甲 | 乙 | 丙 |
| A | NH3 | CuO | 稀HNO3 |
| B | Al | 盐酸 | Fe2O3 |
| C | Si | O2 | H2 |
| D | SO2 | NaOH溶液 | 新制氯水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 电离常数(25℃) |
| 碳酸 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| 次溴酸 | Ka=2.4×10-9 |
| A. | HBrO+Na2CO3═NaBrO+NaHCO3 | B. | 2HBrO+Na2CO3═2NaBrO+H2O+CO2↑ | ||
| C. | HBrO+NaHCO3═NaBrO+H2O+CO2↑ | D. | NaBrO+NaHCO3═Na2CO3+HBrO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com