
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )
A.①②
B.①②④
C.②③
D.①③④
科目:高中化学 来源: 题型:
【题目】(2015·上海)研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )
A.d为石墨,铁片腐蚀加快
B.d为石墨,石墨上电极反应为:O2 + 2H2O + 4e → 4OH–
C.d为锌块,铁片不易被腐蚀
D.d为锌块,铁片上电极反应为:2H+ + 2e → H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.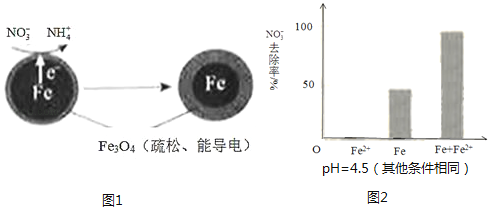
(1)Fe还原水体中NO3﹣的反应原理如图1所示.
①作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: .
(4)其他条件与(2)相同,经1小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3﹣去除率和铁的最终物质形态不同的原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在.由于金红石熔点高,为金属Ti的直接制备带来了困难.在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法.金红石转化成TiCl4的反应方程式如下:TiO2+2C+2Cl2═TiCl4+2CO
(1)用双线桥法标出上述化学方程式的电子转移情况;
(2)指出该反应的氧化剂 , 氧化产物;
(3)当消耗标准状况下Cl211.2L时,则转移的电子数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中氧原子数目与6.8gH2O2中氧原子数目一定相等的是( )
A.6.72L CO
B.6.6gCO2
C.8gSO3
D.9.8gH2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是冶炼铜及制备铁氧化物的重要矿藏,常含微量的金、银等.右图是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程图: 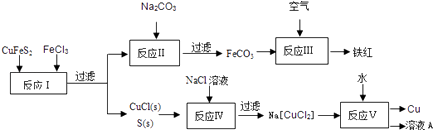
(1)CuFeS2中,Fe的化合价为 .
(2)写出“反应Ⅰ”的离子方程式 , 该反应的氧化剂是 .
(3)CuCl难溶于水,但可与过量的Cl﹣反应生成溶于水的[CuCl2]﹣ . 该反应的离子方程式为 .
(4)反应Ⅰ~V五个反应中属于非氧化还原反应的是反应(选填“Ⅰ~V”).
(5)已知Cu+在反应V中发生自身氧化还原反应,歧化为C u2+和Cu,由此可推知“溶液A”中的溶质为(写出化学式).
(6)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程反应的离子方程式为
(7)将一定量的铁红溶于160mL 5molL﹣1盐酸中,再加入足量铁粉,待反应结束共收集到气体2.24L(标准状况),经检测溶液中无Fe3+ , 则参加反应的铁粉的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碱溶液A、盐溶液B按如下程序进行实验,根据下述现象判断: 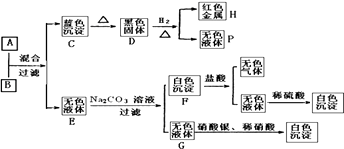
(1)A和B中溶质的化学式A;B、 .
(2)完成下列转化的化学方程式,是离子反应的只写离子方程式.
①A+B→C+E:;
②D+H2→H+P:;
③E+Na2CO3→F+G:;
④F+盐酸→I+E: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO2-+H2O。下列说法不正确的是( )
A. 该电池的优点是电极材料和电解质用完后可以更换
B. 该电池发生氧化反应的是金属铝
C. 电极的正极反应式为3ClO-+3H2O+6e-=3Cl-+6OH-
D. 当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com