


科目:高中化学 来源: 题型:阅读理解
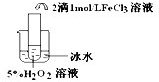
| 实验目的 | 探究温度对H2O2分解反应速率的影响 探究温度对H2O2分解反应速率的影响 | ||||||||||
实验 |
 |
 |
 | ||||||||
| 实验结论 | 结论: 温度越高,反应速率越快 温度越高,反应速率越快 FeCl3在实验中的作用为: 催化剂 催化剂 | ||||||||||
| 反应方程式 | 2H2O2
2H2O2
| ||||||||||
| 实验目的 | 探究卤素单质氧化性的相对强弱 | |
| 实验 | 现象 | 离子方程式 |
| 1.将少量氯水分别加入盛有KBr和NaI溶液的试管中, 振荡后加入CCl4,振荡、静置 |
(1)溶液分层,上层几 乎无色,下层为橙色. (2) 溶液分层,上层几乎无色,下层为紫(红)色 溶液分层,上层几乎无色,下层为紫(红)色 |
(1) Cl2+2Br-=Br2+2Cl- Cl2+2Br-=Br2+2Cl- (2) Cl2+2I-=I2+2Cl- Cl2+2I-=I2+2Cl- |
| 2.将少量溴水加入盛有NaI溶液的试管中, 振荡后加入少量CCl4,振荡、静置 |
/ | (3) Br2+2I-=I2+2Br- Br2+2I-=I2+2Br- |
| 实验结论并从原子结构上解释原因 | 结论:氧化性:Cl2>Br2>I2 解释原因:同主族元素从上到下,核电荷数逐渐增大,电子层数逐渐增多,原子半径逐渐增大,原子核对外层电子的引力逐渐减弱,单质的氧化性逐渐减弱 结论:氧化性:Cl2>Br2>I2 解释原因:同主族元素从上到下,核电荷数逐渐增大,电子层数逐渐增多,原子半径逐渐增大,原子核对外层电子的引力逐渐减弱,单质的氧化性逐渐减弱 | |

查看答案和解析>>
科目:高中化学 来源: 题型:
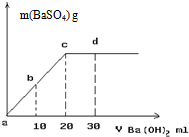 (1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题:
(1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题:查看答案和解析>>
科目:高中化学 来源:2013届山东省德州市跃华学校高三暑假作业过关考试化学试卷(带解析) 题型:实验题
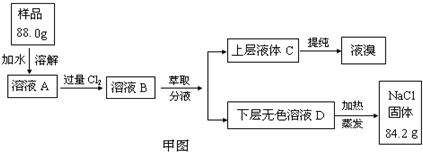
(22分)某中学化学兴趣小组想制取饱和氯水,并进行氯水的性质实验。他们使用如图装置制取较多量的饱和氯水,请回答:
(1)写出仪器的名称:A_________, B _________ 。
(2)写出丙、丁装置中发生反应的离子方程式:
丙_________________________________________________。
丁_________________________________________________。
(3)有同学提出如下改进建议:
①在乙和丙之间增加上图中的a装置,你认为有无必要_______ (填“有”或“无”)。
②在丙的长导管下口处,接上图中的b装置,可以提高氯气的吸收效果。原因是_______________________________ ____。
(4)用制得的氯水分别进行下列实验:①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的粒子是_____;
②滴入AgNO3溶液中,发生反应的离子方程式____________________________________。
(5)用滴管将制得的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然褪去。产生上述现象的原因可能有两种(简要文字说明):
①是由于__________________________________________;
②是由于__________________________________________。
用实验证明红色褪去的原因是①或者②的实验方法是__ ___
。
(6)为了提高氯水中次氯酸的浓度,增强氯水的漂白能力,可向氯水中加入的试剂_____(填序号)。
| A.CaCO3 | B.Na2SO3 | C.H2SO4 | D.Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省高三暑假作业过关考试化学试卷(解析版) 题型:实验题
(22分)某中学化学兴趣小组想制取饱和氯水,并进行氯水的性质实验。他们使用如图装置制取较多量的饱和氯水,请回答:
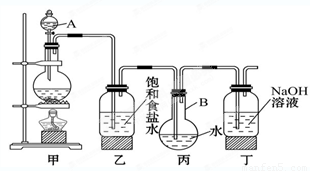
(1)写出仪器的名称:A_________, B _________ 。
(2)写出丙、丁装置中发生反应的离子方程式:
丙_________________________________________________。
丁_________________________________________________。
(3)有同学提出如下改进建议:
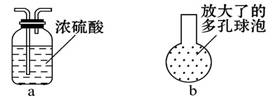
①在乙和丙之间增加上图中的a装置,你认为有无必要_______ (填“有”或“无”)。
②在丙的长导管下口处,接上图中的b装置,可以提高氯气的吸收效果。原因是_______________________________ ____。
(4)用制得的氯水分别进行下列实验:①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的粒子是_____;
②滴入AgNO3溶液中,发生反应的离子方程式____________________________________。
(5)用滴管将制得的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然褪去。产生上述现象的原因可能有两种(简要文字说明):
①是由于__________________________________________;
②是由于__________________________________________。
用实验证明红色褪去的原因是①或者②的实验方法是__ ___
。
(6)为了提高氯水中次氯酸的浓度,增强氯水的漂白能力,可向氯水中加入的试剂_____(填序号)。
A.CaCO3 B.Na2SO3 C.H2SO4 D.Ca(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com