
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )
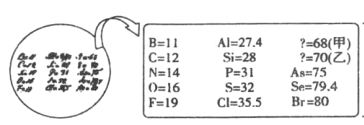
A.推测乙可以用作半导体材料
B.原子半径比较:甲>乙![]()
C.元素乙的简单气态氢化物的稳定性比![]() 弱
弱
D.元素甲的原子序数为21
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】MgCl2·6H2O可用于医药、农业等领域。一种用镁渣[含有MgCO3、Mg(OH)2、CaCO3、Fe2O3和SiO2]制备MgCl2·6H2O的实验流程如下:

(1)“煅烧”只有MgCO3、Mg(OH)2发生分解。“煅烧”须用到下列仪器中的________(填字母)。
A. 蒸发皿 B. 坩埚 C. 泥三角
(2) “蒸氨”在如图所示装置中进行(NH4Cl溶液仅与体系中的MgO反应)。

①三颈烧瓶中发生主要反应的离子方程式为______________。
②倒扣漏斗的作用是________________。
③烧杯中溶液红色深浅不再变化可判断“蒸氨”已完成,其原因是________________。
(3) “过滤”所得滤液经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。向所得产品中加入蒸馏水,测得溶液呈碱性,其可能原因是_________________。
(4) 请补充完整以“滤渣”为原料,制取FeSO4溶液的实验方案:边搅拌边向滤渣中加入1.0 mol·L-1盐酸,_________,得FeSO4溶液(实验中必须用的试剂:1.0 mol·L-1 NaOH溶液、1.0 mol·L-1 H2SO4溶液、铁粉、蒸馏水)。
已知部分金属离子形成氢氧化物沉淀的pH范围如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Ca2+ | 11.3 | — |
Mg2+ | 8.4 | 10.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在800℃时,2L密闭容器内发生反应:2NO(g)+O2(g)2NO2(g),反应体系中,一氧化氮的物质的量随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)如图表示NO2的物质的量浓度变化的曲线是________。

(2)用O2表示从0~2 s内该反应的平均速率v=__________。
(3)能说明该反应已达到平衡状态的是________。
A.v(NO2)=2v(O2)
B.容器内压强保持不变
C.容器内气体质量不变
D.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠(Na2O2)是一种淡黄色固体,有两个实验小组的同学为探究其与二氧化碳的反应,都用下图所示的装置进行实验。一段时间后,将带余烬的木条插入试管D中,木条复燃。
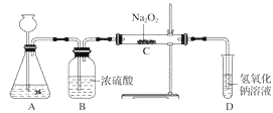
请回答下列问题:
(1)A是制取CO2的装置,写出A中发生反应的化学方程式:__________。
(2)第1小组同学认为Na2O2与CO2反应生成了Na2CO3和O2,该反应的化学方程式为________。
(3)第2小组同学认为除生成Na2CO3和O2外,还有可能生成NaHCO3,你认为呢?并简述原因_____。
(4)请设计一种实验方案证明Na2O2与CO2反应生成了Na2CO3: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是( )

A. 反应C(s)+H2O(g)![]() CO(g)+H2(g) 能量增加(b-a) kJ·mol-1
CO(g)+H2(g) 能量增加(b-a) kJ·mol-1
B. 该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C. 1mol C(s)和1mol H2O(l)反应生成1mol CO(g)和1mol H2(g)吸收热量131.3 kJ
D. 1 mol C(g)、2 mol H、1 mol O转变成1 mol CO(g)和1 mol H2(g)放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,下列情况表明反应A(s)+2B(g)![]() C(g)+D(g) 已达到反应限度的是
C(g)+D(g) 已达到反应限度的是
A. 混合气体的密度保持不变B. 有1mol C生成的同时有1mol D生成
C. 混合气体的总物质的量保持不变D. 有1 mol A生成的同时有1mol C消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照下图所示的操作步骤,完成氢氧化钠与盐酸的反应的实验。

回答下列问题:
(1)反应后混合溶液的温度与反应前盐酸和氢氧化钠溶液的温度相比较其变化是___________________________________。
(2)你认为酸碱中和反应是放热反应还是吸热反应____________________________________。
(3)写出该反应的离子方程式:____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料![]() ,其工艺流程如图所示:
,其工艺流程如图所示:
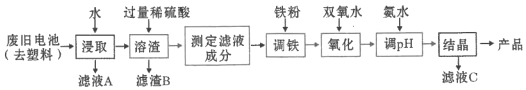
(1)碱性锌锰电池的工作原理:________![]() ________
________![]() ________
________![]() ________
________![]() ________(配平方程式),其中的电解质溶液是
________(配平方程式),其中的电解质溶液是![]() 溶液。滤液
溶液。滤液![]() 中主要溶质的电子式为______。
中主要溶质的电子式为______。
(2)已知![]() 中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将![]() 价锰的化合物全部还原成
价锰的化合物全部还原成![]() ,写出该反应的离子方程式________。
,写出该反应的离子方程式________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式![]() 相符合。
相符合。
①写出“调铁”工序中可能发生反应的离子方程式________,________。
②若“测定滤液成分”结果为![]() ,
,![]() ,滤液体积为
,滤液体积为![]() ,“调铁”工序中,需加入的铁粉质量为________
,“调铁”工序中,需加入的铁粉质量为________![]() (忽略溶液体积变化,用含
(忽略溶液体积变化,用含![]() 、
、![]() 的代数式表示)。
的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是把![]() 氧化为
氧化为![]() ;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是________。
(6)从滤液![]() 中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将8.96 L氯化氢气体溶于水形成100 mL溶液,然后与足量的铁屑反应。
(1)所得盐酸溶液的物质的量浓度是多少________?
(2)参加反应的铁的质量是多少________?
(3)标况下生成氢气的体积是多少________?
(4)将生成的氯化亚铁配成400 mL溶液,此溶液中氯化亚铁的物质的量浓度是多少________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com