
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。常温常压下,E单质是淡黄色固体,常在火山口附近沉积。
(1)D在元素周期表中的位置为____________,C和E离子半径大小比较______________。
(2)A2E的燃烧热ΔH = -a kJ/mol,写出A2E燃烧反应的热化学方程式:_______________。
(3)CA的电子式为 ___________;AB形成的晶体熔点_______。(填“大于”“小于”或“无法判断”)CE形成的晶体熔点。
(4)甲、乙、丙分别是B、D、E三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同。写出向丙溶液中缓慢滴加过量的乙溶液过程中反应的离子方程式:________ 。
(1)第三周期 ⅢA族; Na+<S2- (2)Na+[:H]- 小于
(3)H2S(g)+3/2O2(g)=SO2(g)+H2O(l) △H=-akJ/mol
(4)4H++AlO2-=Al3++2H2O Al3++3AlO2-+6H2O=4Al(OH)3↓
解析试题分析:根据题意可知A是H;B是C;C是Na;D是Al; E是S。(1)Al原子序数为13,核外电子排布为2、8、3,在元素周期表中位于第三周期第ⅢA。Na+核外电子排布为2、8;S2-核外电子排布为2、8、8,对于电子层结构不同的离子来说,离子核外的电子层数越多,离子半径越大。所以这两种离子的半径大小关系为r(Na+)<r(S2-).(2)H2S燃烧反应的热化学方程式为H2S(g)+3/2O2(g)=SO2(g)+H2O(l) △H=-akJ/mol。(3)NaH是离子化合物,其电子式为Na+[:H]-。C、H两元素可以形成CH4、C2H4、C2H2等多种共价化合物,它们都是通过分子间作用力结合而成的分子晶体;而Na、S形成的化合物Na2S是通过离子键结合而成的离子晶体。由于离子键是一种强烈的相互作用,断裂需要消耗较高的能量。所以熔点、沸点比前者形成的分子晶体高很多。(4)根据题意可知甲、乙、丙分别是Na2CO3、NaAlO2、NaHSO4. 向NaHSO4溶液中缓慢滴加过量的NaAlO2溶液过程中反应的离子方程式为4H++AlO2-=Al3++2H2O、Al3++3AlO2-+6H2O=4Al(OH)3↓。
考点:考查元素的推断;元素的位置、结构、性质的关系;离子半径的比较、电子式、化学方程式、离子方程式及热化学方程式的书写等知识。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。
| 元素 | 信息 |
| B | 其单质在常温下为双原子分子,与A可形成分 子X,X的水溶液呈碱性 |
| D | 其简单阳离子与X具有相同电子数,且是同周 期中简单阳离子中半径最小的 |
| E | 元素原子最外层比次外层少2个电子 |
| C、F | 两种元素的原子最外层共有13个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
部分中学化学常见元素原子结构及性质如表所示:
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的 |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
I.已知几种元素原子的价电子构型为3s2,4s2,4s24p1,3d54s2,3s23p3,它们分别属于第几周期?第几族?最高化合价是多少?各元素符号分别是什么?
Ⅱ.第四周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7,其原子序数依次增大。已知A与B 的次外层电子数均为8,而C与D的次外层电子数均为18。根据原子结构,判断:
(1)A、B、C、D的元素符号分别是________、________、________、________。
(2)写出D与A的简单离子的电子排布式________,________。
(3)哪一种元素的氢氧化物碱性最强?__________________________________________。
(4)B与D两原子间能形成何种化合物?________________。写出化学式及电子式________________,________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系。回答下列问题:
(1) 若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的气态化合物分子, Y基态原子的轨道表示式为 ,甲的电子式为
(2)若X原子的价电子排布为ns(n-1)np(n+2),常温下Y为易挥发的液体物质、乙为无色易溶于水的气体。则Z为 ,组成Y的元素的基态原子的电子排布式为 。
(3)若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为: ,Y2+离子的电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
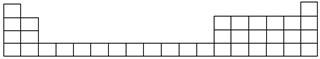
元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为 ;
(2)B元素的负一价离子的电子层结构都与氩相同,B的原子结构示意图为
(3)C元素是第三周期中无未成对电子的主族元素,它的轨道排布式为 ;
(4)D元素基态原子的M层全充满,N层只有一个未成对电子,D基态原子的电子排布式为
(5)E原子共有3个价电子,其中一个价电子位于第三能层d轨道,指出该元素在周期表中所处的周期数和族序数
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。
(2)表中所列元素,属于短周期元素的有________,属于主族元素的有________;g元素位于第________周期第________族;i元素位于第________周期第________族。
(3)元素f是第________周期第________族元素,请在右边方框中按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素。A与B,C、D与E分别位于同一周期。A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体。
(1)写出A元素的基态原子价电子排布式__________;F离子电子排布式为__________。
(2)写出X的化学式__________________________,化学名称为_________________。
(3)写出X涉及金属冶炼中的一个化学方程式_______________________________。
(4)试解释工业冶炼D不以DE3而是以D2A3为原料的原因:
________________________________________________________________________。
(5)CE、FA的晶格能分别为786 kJ·mol-1、3 401 kJ·mol-1,试分析导致两者晶格能差异的主要原因是_______________________________________
(6)F与B可形成离子化合物,其晶胞结构如图所示:F与B形成离子化合物的化学式为________;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是________________(只要求列出算式)。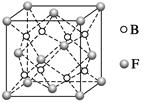
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com