
分析 氧化铁和氧化铝分别和盐酸反应生成氯化铁、氯化铝和水,向氯化铝溶液中滴加足量氢氧化钠溶液,可观察到溶液中的现象是先产生白色沉淀氢氧化铝,然后白色沉淀氢氧化铝逐渐消失生成偏铝酸钠,向氯化铁溶液中滴加氢氧化钠,氢氧化钠和氯化铁溶液反应生成红褐色氢氧化铁沉淀;
解答 解:氧化铁和盐酸反应方程式为Fe2O3+6HCl=2FeCl3+3H2O,氧化铝和盐酸反应方程式为:Al2O3+6HCl=2AlCl3+3H2O,所以二者得到的盐分别是FeCl3、AlCl3,向氯化铝溶液中滴加足量氢氧化钠溶液,可观察到溶液中的现象是先产生白色沉淀氢氧化铝,AlCl3+3NaOH=Al(OH)3↓+3NaCl,然后白色沉淀氢氧化铝逐渐消失生成偏铝酸钠,Al(OH)3+NaOH=NaAlO2+2H2O,向氯化铁溶液中滴加氢氧化钠,氢氧化钠和氯化铁溶液反应,立即生成红褐色氢氧化铁沉淀,FeCl3+3NaOH=Fe(OH)3↓+3NaCl,所以看到的现象是产生红褐色沉淀,故选②,
故答案为:FeCl3;AlCl3;AlCl3;②;
点评 本题考查了氧化铁、氧化铝、铁、铝发生的化学反应,明确物质的性质是解本题关键,根据物质的性质来分析解答,注意氧化铁和盐酸反应生成氯化铁而不是氧化亚铁,注意比较氯化亚铁、氯化铁分别和氢氧化钠溶液反应现象的不同,为易错点,题目较简单.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
 所示,下列说法正确的是( )
所示,下列说法正确的是( )| A. | 该有机物的分子式为C8H8O3 | |
| B. | 1 mol该有机物最多能与2 mol H2发生加成反应 | |
| C. | 该有机物能发生加成反应,取代反应和氧化反应 | |
| D. | 该有机物的一种芳香族同分异构体能含一个羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应是旧键断裂和新键形成的过程 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ①② | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
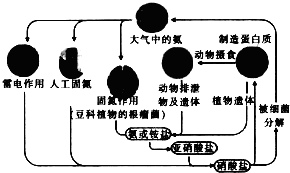
| A. | 含氮无机物和含氮有机物可相互转化 | |
| B. | 通过闪电产生NO属于高能固氮 | |
| C. | 硝酸盐被细菌分解为氮气过程氮元素一定被氧化 | |
| D. | C、H、O也参与自然界中氮循环 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
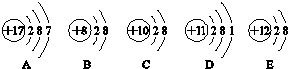
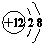 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g O3含有的氧原子数为NA | |
| B. | 常温常压下,22.4L SO2含有的分子数为NA | |
| C. | 1molMg变成Mg2+时,失去电子的数目为NA | |
| D. | 1L 1mol•L-1H2SO4溶液中含H+的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com