

| 实验编号 | 操作 | 现象及结论 |
| a | 加入2mL蒸馏水,再加入10mL 5mol/L Na2S2O8溶液,振荡 | 红色固体逐渐溶解,先慢后快. |
分析 根据实验原理可知,用(NH4)2S2O8和氢氧化钠反应生成Na2S2O8,由于NH3能与Na2S2O8反应,所以实验中要用氮气把生成的氨气及明排出容器,生成的氨气可以用硫酸吸收,氨气极易溶于水,所以要用防倒吸装置,
(1)根据上面的分析可知,装置Ⅱ是吸收氨气尾气的;
(2)根据装置图可知仪器名称;根据题意该反应是在55℃条件下进行,所以要用水浴加热;
(3)NH3能与Na2S2O8反应,所以要及时排出;
(4)用惰性电极如铂电解KHSO4溶液,阳极上HSO4-被氧化生成过硫酸根,根据电荷守恒和元素守恒书写电解反应式;
(5)Na2S2O8溶液与铜只生成两种盐,根据电子得失守恒和元素守恒可知,这两种物质应为硫酸钾和硫酸铜,据此书写化学方程式;根据影响反应速率的因素推断甲反应为放热反应;
解答 解:(1)根据上面的分析可知,装置Ⅱ是吸收氨气尾气的,
故答案为:吸收NH3;
(2)根据装置图可知装置I中盛NaOH溶液的仪器名称是分液漏斗,根据题意该反应是在55℃条件下进行,所以要用水浴加热,要用到温度计、酒精灯、盛热水浴的水槽,故选abc,
故答案为:分液漏斗;abc;
(3)NH3能与Na2S2O8反应,所以要及时排出,所以需要持续通入N2的目的是使三颈烧瓶内产生的NH3及时排除,减少副反应②的发生,
故答案为:使三颈烧瓶内产生的NH3及时排除,减少副反应②的发生;
(4)用惰性电极如铂电解KHSO4溶液,阳极上HSO4-被氧化生成过硫酸根,反应的化学反应式为2KHSO4$\frac{\underline{\;电解\;}}{\;}$ K2S2O8+H2↑,
故答案为:2KHSO4$\frac{\underline{\;电解\;}}{\;}$ K2S2O8+H2↑;
(5)Na2S2O8溶液与铜只生成两种盐,根据电子得失守恒和元素守恒可知,这两种物质应为硫酸钾和硫酸铜,化学方程式为K2S2O8+Cu=K2SO4+CuSO4,根据影响反应速率的因素推断甲反应为放热反应,
故答案为:K2S2O8+Cu=K2SO4+CuSO4;放热.
点评 本题考查物质制备及性质实验的操作,明确制取的原理以及氯气的性质等是解题关键,题目综合性强,难度较大.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应是氧化还原反应 | |
| B. | 该反应的△H<0 | |
| C. | 生成新物质的化学式为 Fe2S3 | |
| D. | 生成新物质的总能量低于反应物铁粉和硫粉的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验步骤 | 实验现象 | 结论 |
| Ⅰ | 在两个蒸发皿中各加入10mL冷水,控制相同燃烧条件,分别用乙醇和汽油作为燃料进行加热,记录从开始到水沸腾的时间. | 用乙醇加热耗时118s;用汽油加热耗时56s. | 猜想2不成立 (填“成立”或“不成立”) |
| Ⅱ | 实验Ⅰ停止加热后,取下蒸发皿,观察蒸发皿的底部. | 用乙醇加热的蒸发皿底部只有及少量炭黑,而用汽油加热的蒸发皿底部有大量的炭黑. | 猜想1成立(可仿照上格填写) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 | 1.200 | 1.000 | 0.800 | 0.600 |
| 270 | 3.60 | 3.00 | 2.40 | 1.80 |
| 280 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
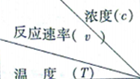
| A. | 升高温度或增大A的浓度都可以增大v的值 | |
| B. | 同时改变反应温度和A的浓度,v可能不变 | |
| C. | a=6.00 | |
| D. | 270<b<280 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
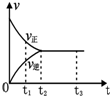 如图是可逆反应N2(g)+3H2(g)?2NH3(g)在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应N2(g)+3H2(g)?2NH3(g)在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,只有正反应在不断进行,速率在逐渐减小 | |
| B. | t2时,反应到达限度,在此条件下N2的转化率达到最大 | |
| C. | t2-t3,反应不再发生,各物质的物质的量保持恒定 | |
| D. | t3以后,N2(g)、H2(g)、NH3(g)的物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
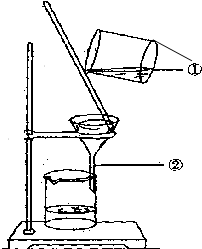 如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
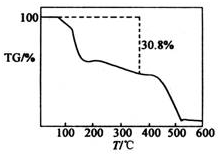 硫酸锰铵[(NH4)2SO4•MnSO4•nH2O]是浅粉色晶体,易溶于水,在农业上用作微量元素肥料.实验室由MnO2制备硫酸锰铵的实验步骤如下:
硫酸锰铵[(NH4)2SO4•MnSO4•nH2O]是浅粉色晶体,易溶于水,在农业上用作微量元素肥料.实验室由MnO2制备硫酸锰铵的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能加快反应速率的主要原因,是增加了反应物分子中活化分子的百分数 | |
| B. | 正反应是吸热反应,达到平衡时,升高温度,v正增大,v逆减小,所以平衡向正反应方向移动 | |
| C. | 一定条件下增大反应物的量,一定会加快反应速率 | |
| D. | 对于任何一个化学反应,用其中任何一种反应物浓度的减小来表示化学反应速率,都是相同的数值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com