
【题目】色酮类化合物K具有抗菌、降血脂等生理活性,其合成路线如下:
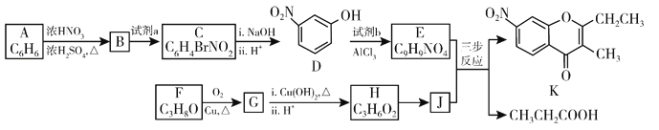
已知:
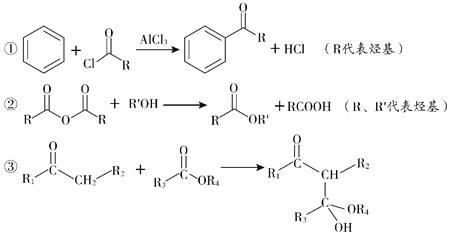
(R、R1、R2、R3、R4代表烃基)
(1)A的结构简式是________;根据系统命名法,F的名称是________。
(2)B→C所需试剂a是________;试剂b的结构简式是____________。
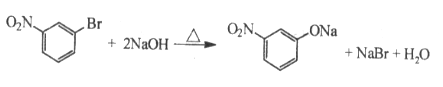
(3)C与足量的NaOH反应的化学方程式为____________。
(4)G与银氨溶液反应的化学方程式为___________。
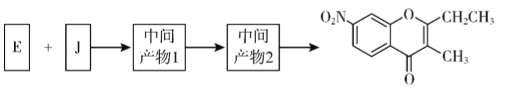
(5)已知:①2H ![]() J+H2O; ②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出下列化合物的结构简式:____________
J+H2O; ②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出下列化合物的结构简式:____________
【答案】 1-丙醇 Br2和Fe(或FeBr3)
1-丙醇 Br2和Fe(或FeBr3) 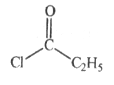
 CH3CH2CHO+2Ag(NH3)2OH
CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3+H2O E:
CH3CH2COONH4+2Ag↓+3NH3+H2O E: ; J:
; J: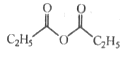 ;
;
中间产物1: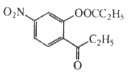 ; 中间产物2:
; 中间产物2: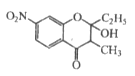
【解析】
A的分子式是C6H6,结构简式为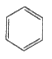 ,A发生硝化反应生成B,B为
,A发生硝化反应生成B,B为![]() ,由D的结构简式及反应条件,可知C为
,由D的结构简式及反应条件,可知C为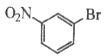 。F的分子式是C3H8O,能催化氧化生成醛基,则含有—CH2OH结构,结构简式为CH3CH2CH2OH,F催化氧化生成G,G为CH3CH2CHO,G催化氧化生成H,H为CH3CH2COOH,以此分析。
。F的分子式是C3H8O,能催化氧化生成醛基,则含有—CH2OH结构,结构简式为CH3CH2CH2OH,F催化氧化生成G,G为CH3CH2CHO,G催化氧化生成H,H为CH3CH2COOH,以此分析。
A的分子式是C6H6,结构简式为 ,A发生硝化反应生成B,B为
,A发生硝化反应生成B,B为![]() ,由D的结构简式及反应条件,可知C为
,由D的结构简式及反应条件,可知C为 。F的分子式是C3H8O,能催化氧化生成醛基,则含有—CH2OH结构,结构简式为CH3CH2CH2OH,F催化氧化生成G,G为CH3CH2CHO,G催化氧化生成H,H为CH3CH2COOH,
。F的分子式是C3H8O,能催化氧化生成醛基,则含有—CH2OH结构,结构简式为CH3CH2CH2OH,F催化氧化生成G,G为CH3CH2CHO,G催化氧化生成H,H为CH3CH2COOH,
(1)根据以上分析,A的结构简式是 ;F的结构简式为CH3CH2CH2OH,名称是1-丙醇。
;F的结构简式为CH3CH2CH2OH,名称是1-丙醇。
故答案为:  ;1-丙醇;
;1-丙醇;
(2) B→C是苯环上的溴代反应,则试剂a为Br2和Fe(或FeBr3);由D的结构简式和已知①,可知试剂b为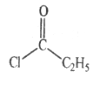 。
。
故答案为:Br2和Fe(或FeBr3); ;
;
(3)C与足量的NaOH反应为卤代烃的水解反应和酸碱中和反应,化学方程式为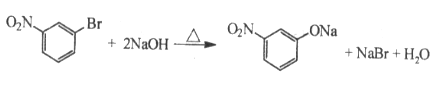 。
。
故答案为: 。
。
(4)G与银氨溶液发生醛基的氧化反应,化学方程式为CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3+H2O 。
CH3CH2COONH4+2Ag↓+3NH3+H2O 。
故答案为:CH3CH2CHO+2Ag(NH3)2OH ![]() CH3CH2COONH4+2Ag↓+3NH3+H2O;
CH3CH2COONH4+2Ag↓+3NH3+H2O;
(5)根据(5)中已知条件可知,E为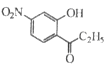 ,J为丙酸酐,结构简式为
,J为丙酸酐,结构简式为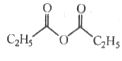 ;根据已知②可得中间产物1为
;根据已知②可得中间产物1为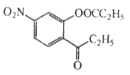 ,根据已知③可得中间产物2为
,根据已知③可得中间产物2为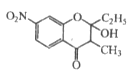 。
。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】某些芳香族化合物的分子式均为C7H8O,其中与FeCl3溶液混合后,显紫色和不显紫色的种类分别为( )
A.2种和1种B.2种和3种C.3种和2种D.3种和1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,![]() 与R-发生如下反应
与R-发生如下反应![]() +5R-+6H+=3R2+3H2O,下列有关R元素的叙述正确的是( )
+5R-+6H+=3R2+3H2O,下列有关R元素的叙述正确的是( )
A. R是第ⅤA族元素 B. R2在常温下一定是气体
C. ![]() 中的R元素只能被还原 D. R的氢化物的水溶液是强酸
中的R元素只能被还原 D. R的氢化物的水溶液是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A.金刚石、B.MgF2、C.NH4Cl、D.NaNO3、E.干冰、F.固体碘,填写下列空白。(用序号填写)
(1)熔化时不需破坏化学键的是________,熔化时只需破坏共价键的是________,熔点最低的是________,
晶体中既存在离子键又存在共价键的是________。
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,则1 mol N4生成N2的ΔH=______ kJ·mol-1

(3) 50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH溶液在如图所示的装置中进行中和反应。

请回答下列问题:
从实验装置上看,图中尚缺少的一种玻璃仪器是_____,烧杯间填满碎泡沫塑料的作用是______。大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期;C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙;A原子的最外层电子数比次外层电子数多3个;D周期序数等于D原子最外层电子数;E原子半径是同周期中最小的(除稀有气体外),根据以上信息回答下列问题:
(1)A元素在周期表中的位置__________________;
(2)乙物质中存在的化学键类型是______________;
(3)写出C与D的最高价氧化物对应的水化物相互间反应的离子方程式_____________;
(4)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的有效成分的电子式为_______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 四种元素的单质中,Z单质的熔、沸点最低
D. W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:

根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应________。
(3)D装置的石棉中均匀混有KI粉末,其作用是________________________________________。
(4)E装置的作用是____________(填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式____________________________________。
(6)E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为______(填编号)。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下某溶液中由水电离产生的[H+]=1×10-5mol·L-1,则下列叙述正确的是
A.一定是碱溶液
B.一定是酸溶液
C.由水电离出的[OH-]=1×10-9mol·L-1
D.pH值可能为9也可能为5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(结构简式为![]() )有下列叙述:①不能使酸性KMnO4 溶液褪色;②能使溴的四氯化碳溶液褪色;③不可溶于水;④可溶于苯中;⑤1mol苯乙烯最多能与4molH2发生加成反应;⑥所有的原子不可能共平面,其中正确的是
)有下列叙述:①不能使酸性KMnO4 溶液褪色;②能使溴的四氯化碳溶液褪色;③不可溶于水;④可溶于苯中;⑤1mol苯乙烯最多能与4molH2发生加成反应;⑥所有的原子不可能共平面,其中正确的是
A. ②③④⑤ B. ①②⑤⑥ C. ②③④⑥ D. 全部正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com