
【题目】“绿色化学”的核心是在化学反应过程中或化工生产中,尽量减少使用或彻底消除有害物质,下列做法中,符合“绿色化学”理念的是 ( )
A.生产和使用剧毒农药 B.化工厂产生的废气向高空排放
C.利用氢气作高能燃料 D.造纸厂用二氧化硫进行纸浆漂白
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.稀硫酸滴在银片上:2Ag+2H+===2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)![]() (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)![]() NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3 与 ΔH1、ΔH2 之间的关系是:ΔH3=________。
(2)白磷与氧气反应生成P4O10 固体 。下表所示是部分化学键的键能参数:
化学键 | P—P | P—O | P===O | O===O |
键能/kJ·mol-1 | a | b | c | d |
根据右图的分子结构和有关数据通过计算写出该反应的热化学方程式为 。
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右下图)之间脱去两个水分子产物,其结构式为_________________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为____________。
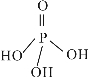
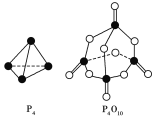
(4)已知298 K时白磷不完全燃烧的热化学方程式为:
P4(s,白磷)+3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。
在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)有以下微粒:①N2H4 ②P4 ③H2O ④N2 ⑤H3O+ ⑥NH4+ ⑦CO2 ⑧H2O2
(填编号)
(1)既有极性键又有非极性键的是 ;(2)既有σ键又有π键的是 ;
(3)微粒中不含孤电子对的是____________;(4)立体构型呈正四面体的是____________;
(5)⑤和⑧的电子式分别为 和 ;
(6)⑥和⑦的结构式分别为 和 ;
(二)以下反应均为放热反应,根据热化学方程式,比较 △H1 和 △H2 的大小
① I2(g)+ H2(g)=2HI(g) △H1;I2(s)+ H2(g)=2HI(g) △H2,则△H1 △H2
② H2(g)+Cl2(g)=2HCl(g) △H1;H2(g)+Br2(g)=2HBr(g) △H2,则△H1 △H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,可行的是( )
A. 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B. 用萃取的方法分离汽油和煤油
C. 用溶解、过滤的方法分离KNO3和NaCl固体的混合物
D. 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)质量之和为96克的O2和O3的气体混合,其氧原子个数为______________。
(2)现要配制1 mol·L1 Na2CO3溶液250 mL,求:①需要固体Na2CO3_____________g;②需要含结晶水的碳酸钠晶体(Na2CO3·10 H2O) g;③需要物质的量浓度为4 mol·L1的Na2CO3溶液 mL;④需要溶质的质量分数为12%、密度为1.12 g·cm-3的Na2CO3溶液 mL。
(3)在配制上述溶液的过程中,可能导致配制溶液浓度偏小的有:_________
A. 固体Na2CO3放在右盘(1 g以下用游码);
B. 容量瓶用碳酸钠溶液先润洗;
C. 转移溶液时未洗涤烧杯;
D. 定容时,溶液未冷却;
E. 定容时视线仰视;
F. 摇匀时,发现液面低于容量瓶刻度线,但未补加水;
G. 容量瓶未干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识填空:
(1)0.3molNH3中所含质子数与______gH2O分子中所含质子数相等。
(2)标准状况下,2.4g某气体的体枳为672mL,则此气体的相对分子质量为__________。
(3)某盐混合溶液中含有离子:Na+、Mg2+、 Cl-、SO42-,测得Na+、Mg2+和C1-的物质的量浓度依次为:0.2mol/L、0.25mol/L、0.4mol/L,测得c(SO42-)=__________。
(4)己知离子反应:RO33-+6I-+6H+=R-+3I2+3H2O,试根据离子方程式必须“质量守恒,电荷守恒”等判断:n=___________,R元素在中RO33-的化合价是_____________。
(5)同温同压下,SO2与O2的密度之比为___________,若质量相同,两种气体的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液)。
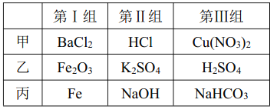
根据该表回答问题:
①第Ⅲ组中有一种物质能与第___________组中的所有物质反应,这种物质是___________。
②第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是___________,该物质能与第Ⅲ组中所有物质发生反应,其离子反应方程式分别为:___________,___________,___________。
(2)现有下列几种物质①铜②稀硫酸③氯化氢④氯气⑤空气⑥二氧化碳⑦盐酸⑧氯化钠⑨熔融的硝酸钾⑩硫酸钡,其中,属于混合物的有_________,(填序号,下同)属于电解质的有________,属于非电解质的有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com