
 恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )
恒容容器中,对于可逆反应xX(g)+yY(g)?zZ(g)+mM(g),x的百分含量随时间的变化如图,下列说法正确的是( )| A. | x+y>z+m | |
| B. | 对反应体系加压v正>v逆 | |
| C. | 该反应正反应方向为热反应 | |
| D. | 对反应体系降低温度达平衡前v逆>v正 |
分析 由曲线可知,温度都为T1时,P1先达到平衡,则P1>P2,而增大压强,X的百分含量增大,说明平衡逆向移动,则x+y<z+m,当压强为P2时,先达到平衡T2,说明T2>T1,升高温度,X的百分含量降低,说明平衡正向移动,则说明正反应为吸热反应,以此解答该题.
解答 解:由曲线可知,温度都为T1时,P1先达到平衡,则P1>P2,而增大压强,X的百分含量增大,说明平衡逆向移动,则x+y<z+m,当压强为P2时,先达到平衡T2,说明T2>T1,升高温度,X的百分含量降低,说明平衡正向移动,则说明正反应为吸热反应,
A.由以上分析可知x+y<z+m,故A错误;
B.增大氧气,平衡逆向移动,则v正<v逆,故B错误;
C.由以上分析可知正反应为吸热反应,故C错误;
D.降低温度,平衡逆向移动,则v逆>v正,故D正确.
故选D.
点评 本题考查了化学平衡图象分析判断,为高频考点,侧重于学生的分析能力的考查,注意把握化学平衡移动原理,注意图象分析方法,先拐先平温度,压强大,题目难度中等.


科目:高中化学 来源: 题型:选择题
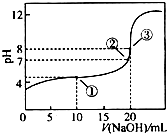 在25℃时,向50.00mL未知浓度的CH3COOH溶液中逐滴加入0.5mol•L-1的NaOH溶液.滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如图所示,则下列说法中,不正确的是( )
在25℃时,向50.00mL未知浓度的CH3COOH溶液中逐滴加入0.5mol•L-1的NaOH溶液.滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如图所示,则下列说法中,不正确的是( )| A. | 该滴定过程可采用酚酞做指示剂 | |
| B. | 图中点③所示溶液中,c(CH3COO-)<c(Na+) | |
| C. | 图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度 | |
| D. | 滴定过程中的某点,会有c(Na+)=c(CH3COO-)>c(H+)=c(OH-)的关系存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的单晶硅用于制造光导纤维 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 乙酸乙酯在碱性条件下水解称为皂化反应 | |
| D. | 可溶性铜盐有毒,在生命体中铜是一种不可缺少的微量元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O;
+3H2O;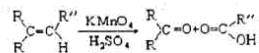

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若增大压强,平衡向正方向移动,平衡常数变大 | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为0.015mol/L | |
| C. | 达到平衡时X浓度为0.04 mol/L | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质参加的化合反应一定是氧化还原反应 | |
| B. | 有单质生成的分解反应一定是氧化还原反应 | |
| C. | 置换反应一定是氧化还原反应 | |
| D. | 有单质参加或生成的反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
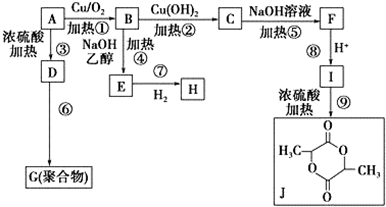
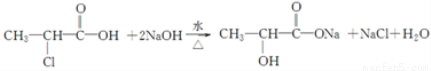 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠存放在盛有煤油的试剂瓶中 | |
| B. | 烧碱盛放在玻璃瓶塞的磨口玻璃瓶中 | |
| C. | 存放液溴的试剂瓶中应加水封 | |
| D. | 漂白粉置于冷暗处密封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com