
 I����1�����ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��ͼ��t1 ʱ����ƽ���ƶ�����������������ѹǿ��
I����1�����ϳɰ���Ӧ�ﵽƽ��ı�ijһ������������ı�N2��H2��NH3����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��ͼ��t1 ʱ����ƽ���ƶ�����������������ѹǿ������ I��1������ͼ�����Ӱ��ƽ������أ���Ҫ�Ƿ�Ӧ���з�������ʵı仯����������
��2����ѧƽ�ⳣ������������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��������ʽ���м��㣻
��3�����Ũ���̣���ѧƽ�ⳣ������ƽ�����淴Ӧ�����ƶ������Ũ���̣�ƽ�ⳣ������ƽ��������Ӧ�����ƶ������Ũ����=��ѧƽ�ⳣ������ƽ�ⲻ�ƶ���
II����1�������ɳ�����Ӧ����c��Cu2+����c2��OH-����2��10-20��c��Cu2+��=0.02mol/L���ɼ���c��OH-������������pH��
��2����ѧ��Ӧ�У���ѧ�����������������γ��»�ѧ���ų����������ݷ���ʽ����ֱ����պͷų����������Դ˼��㷴Ӧ�Ȳ��ж����Ȼ��Ƿ��ȣ�
��3���ȸ�������η��࣬�ٸ����������ǿ�����࣬�����ε�ˮ�������Է���Ƚϣ�
��� �⣺I��1���ɷ�Ӧ������ʱ��Ĺ�ϵͼ���֪��t1ʱ���淴Ӧ���ʶ�����ƽ�������ƶ�������ƽ���ƶ�����������������ѹǿ��
�ʴ�Ϊ������ѹǿ��
��2��N2��g��+3H2��g��?2NH2��g��
��ʼ amol/L 4amol/L 0
��Ӧ amol/L 3amol/L 2amol/L
ƽ�� amol/L amol/L 2amol/L
���Ի�ѧƽ�ⳣ��K=$\frac{��2amol/L��^{2}}{��amol/L��•��amol/L��^{3}}$=$\frac{4}{{a}^{2}}$��L/mol��2��
�ʴ�Ϊ��$\frac{4}{{a}^{2}}$��L/mol��2��
��3��Ũ����=$\frac{{2}^{2}}{1��{3}^{2}}$=0.1481��0.12����ƽ�����淴Ӧ�����ƶ�����ѡB��
�ʴ�Ϊ��B��
II����1�������ɳ�����Ӧ����c��Cu2+����c2��OH-����2��10-20��c��Cu2+��=0.02mol/L����c��OH-��=$\sqrt{\frac{2��1{0}^{-20}}{0.02}}$mol/L=10-9mol/L����c��H+��=10-5mol/L��pH=5��
�ʴ�Ϊ��5��
��2���ڷ�ӦN2+3H2?2NH3�У�����3molH-H����1mol N��N�������յ�����Ϊ��3��436kJ+946kJ=2254kJ������2mol NH3�����γ�6mol N-H�����ų�������Ϊ��6��391kJ=2346kJ�����յ������٣��ų��������࣬�÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ��2346kJ-2254kJ=92kJ��
�ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92kJ•mol-1��
��3���CH3COOH ��������ʣ�����ֻ�в��ֵ��룬��C��H +����0.1mol/L������PH��1��
���NaOH����Ba��OH��2 ��Ũ����ͬʱ�����Լ�pHΪ�ޣ��ݣ�PH��7��
�Σ���NaHSO4��ǿ����ʽ�Σ���ˮ����ȫ����������ӡ���������ӡ������ӣ�����C��H +��=0.1mol/L������PH=1��
��NH4Cl��ǿ�������Σ�ˮ�����Һ�����ԣ�1��PHֵ��7��
��KNO3��ǿ��ǿ���Σ�ˮ��Һ�����ԣ�PH=7��
��Na2CO3 ��ǿ�������Σ�ˮ��Һ���ʼ��ԣ���̼���Ƶ�ˮ��̶ȴ���̼�����Ƶ�ˮ��̶ȣ�����̼������Һ�ļ��Դ���̼��������Һ�ļ��ԣ�
�ʴ�Ϊ���ޣ��ݣ��ڣ��٣��ߣ��ܣ��ۣ�
���� ���⿼����Ӱ�컯ѧ��Ӧ���ʵ����أ�ͼ���������ѧƽ������ʽ���㣬�Ȼ�ѧ����ʽ����д��֪ʶ�㣬ע��֪ʶ��Ǩ�ƺ�Ӧ���ǹؼ����ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +
+ $\stackrel{��}{��}$
$\stackrel{��}{��}$
 b��
b�� c��
c��
 ��
�� ��
�� ��
�� ��д����ϳ�·�ߣ�
��д����ϳ�·�ߣ� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ3��Heԭ�ӣ�32He | B�� | HCl�ĵ���ʽ�� | ||
| C�� | S2-�Ľṹʾ��ͼ�� | D�� | �£�N2H4���Ľṹ��ʽ��H2N-NH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl2��Һ��ͨ��������Fe2++Cl2=Fe3++2Cl- | |
| B�� | FeS�������ϡ������Һ�У�FeS+2H+=Fe2++H2S�� | |
| C�� | ̼����þ������������������Һ��Ӧ��Ca2++OH-+HCO3-=CaCO3��+H2O | |
| D�� | ��������Һ�еμ�Ba��OH��2��Һ��ǡ��ʹAl3+������ȫ��2Al3++3SO42-+3Ba2++6OH-=2 Al��OH��3��+3BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������� | �¶ȣ��棩 | |||
| ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |||
| CH3OH��g�� | CH3OCH3��g�� | H2O��g�� | ||
| �� | 387 | 0.20 | 0.080 | 0.080 |
| �� | 387 | 0.40 | ||
| �� | 207 | 0.20 | 0.090 | 0.090 |
| A�� | �÷�Ӧ���淴ӦΪ���ȷ�Ӧ | |
| B�� | �ﵽƽ��ʱ���������е�CH3OH����������������е�С | |
| C�� | �ﵽƽ��ʱ���������е�ѹǿ���������е�ѹǿ��ͬ | |
| D�� | ����ʼʱ���������г���CH3OH 0.15 mol��CH3OCH3 0.15 mol ��H2O 0.10 mol����Ӧ��������Ӧ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ����� | ʱ�� Ũ�� �¶� | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800�� | c3 | 0.92 | 0.75 | 0.60 | 0.60 | 0.60 | 0.60 |
| 4 | 820�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
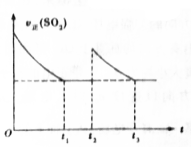 һ���¶��£��ܱ������н��з�Ӧ��2SO2��g��+O2��g��?2SO3��g����H��0�����v����SO2���淴Ӧʱ�䣨t���ı仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������
һ���¶��£��ܱ������н��з�Ӧ��2SO2��g��+O2��g��?2SO3��g����H��0�����v����SO2���淴Ӧʱ�䣨t���ı仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | t2ʱ�ı�������ǣ�ֻ����һ������SO2 | |
| B�� | t1ʱƽ�ⳣ��K1����t3ʱƽ�ⳣ��K2 | |
| C�� | t1ʱƽ��������$\overline{{M}_{1}}$����t3ʱƽ��������$\overline{{M}_{2}}$ | |
| D�� | t1ʱƽ�������е�SO3�������������t3ʱƽ��������SO3��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C6H12O6��������aq��+6O2$\stackrel{ø}{��}$6CO2+6H2O | |
| B�� | CH3COOH+KOH�TCH3COOK+H2O | |
| C�� | A+B�TC+D����H��0 | |
| D�� | Ba��OH��2•8H2O��NH4Cl��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com