
| mg |
| NA |
| m |
| NA |
| m |
| NA |


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ĆÜ¶Č£ŗ1-äå¼×Ķ飼1-äåŅŅĶ飼1-äå±ūĶé |
| B”¢µČĪļÖŹµÄĮæµÄ“¼Óė×ćĮæNa·“Ӧɜ³ÉĒāĘųµÄĮæ£ŗ¼×“¼£¼ŅŅ¶ž“¼£¼±ūČż“¼ |
| C”¢·Šµć£ŗĮŚ¶ž¼×±½£¾¼ä¶ž¼×±½£¾¶Ō¶ž¼×±½ |
| D”¢ŌŚĖ®ÖŠČܽāŠŌ£ŗŅŅ“¼£¾Õż¶”“¼£¾ÕżŹ®¶ž“¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2- 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
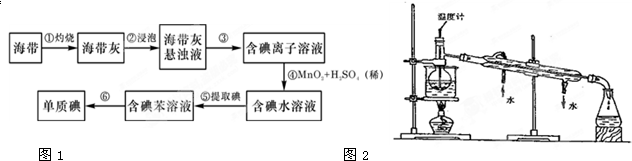
 ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®¾Ż“ĖĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®¾Ż“ĖĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A”¢øĆĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ9.2 mol/L |
| B”¢ČōøĆĮņĖįÓėµČĢå»żµÄĖ®»ģŗĻ£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹżŠ”ÓŚ49% |
| C”¢ČōŹµŃéŹŅŠčŅŖ4.6 mol/LµÄĻ”ĮņĖį480 mL£¬ŌņÓ¦ÓĆĮæĶ²ĮæČ”øĆĮņĖį125.0mL |
| D”¢µČÖŹĮæµÄĖ®ÓėøĆĮņĖį»ģŗĻĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅØ¶Č“óÓŚ9.2 mol/L |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com