
A.µČÓŚ0.23 mol B.“óÓŚ0.23 mol
C.µČÓŚ0.46 mol D.Š”ÓŚ0.46 mol

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
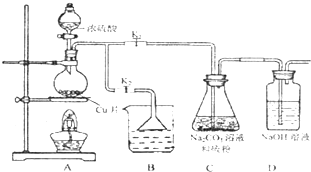 Įņ“śĮņĖįÄĘ£ØNa2S2O3£©æÉÓÉŃĒĮņĖįÄĘŗĶĮņ·ŪĶعż»ÆŗĻ·“Ó¦ÖĘµĆ£®
Įņ“śĮņĖįÄĘ£ØNa2S2O3£©æÉÓÉŃĒĮņĖįÄĘŗĶĮņ·ŪĶعż»ÆŗĻ·“Ó¦ÖĘµĆ£®2- 4 |
2- 7 |
| ±ąŗÅ | 1 | 2 | 3 | 4 |
| ĻūŗÄNa2S2O3±ź×¼ČÜŅŗµÄĢå»ż/mL | 18.02 | 17.98 | 18.00 | 20.03 |
2- 7 |
2- 3 |
2- 6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğÉĻŗ£ŹŠćÉŠŠĒųøßČżÉĻѧʌʌĩ½Ģѧ֏Įæ¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ÉĮŠææó(Ö÷ŅŖ³É·ŻĪŖZnS)ŹĒŗ¬ŠæÖ÷ŅŖæóĪļÖ®Ņ»£¬æÕĘųÖŠøßĪĀ¼ÓČČÉĮŠææóÉś³ÉZnOŗĶSO2”£ZnOÓĆÓŚŅ±Į¶½šŹōŠæ£¬SO2æÉÖĘŃĒĮņĖįŃĪ»ņĮņĖį”£»Ų“šĻĀĮŠĪŹĢā(ŅŌĻĀ¼ĘĖć±£Įō2Ī»Š”Źż)
£Ø1£©Č”1.56 gÉĮŠææóѳʷ£¬ŌŚæÕĘųÖŠøßĪĀ¼ÓČČ(ŌÓÖŹ²»·“Ó¦)£¬³ä·Ö·“Ó¦ŗó£¬ĄäČ“£¬µĆµ½²ŠĮō
¹ĢĢåµÄÖŹĮæĪŖ1.32 g£¬ŃłĘ·ÖŠŗ¬Įņ»ÆŠæµÄÖŹĮæ·ÖŹżŹĒ_________”£
£Ø2£©Č”1.95 gŠæ¼ÓČėµ½12.00 mL 18.4 mol/LµÄÅØĮņĖįÖŠ(·“Ӧ֊ֻɜ³ÉŅ»ÖÖ»¹Ō²śĪļ)£¬³ä·Ö·“Ó¦ŗ󣬊”ŠÄµŲ½«ČÜŅŗĻ”ŹĶµ½1000 mL£¬Č”³ö15.00 mL£¬ŅŌ·ÓĢŖĪŖÖøŹ¾¼Į£¬ÓĆ0.25 mol/LµÄNaOHČÜŅŗÖŠŗĶÓąĖį£¬ŗÄÓĆNaOHČÜŅŗµÄĢå»żĪŖ21.70 mL”£
¢Ł·“Ó¦ŗóČÜŅŗÖŠ¶ąÓąµÄĮņĖįŹĒ____________ mol”£
¢ŚĶعż¼ĘĖćČ·¶ØÅØĮņĖį±»»¹ŌµÄ²śĪļŹĒ________________________”£
£Ø3£©½«±źæöĻĀ4.48 L SO2ĘųĢåĀżĀżĶØČė200 mLŅ»¶ØÅضČNaOHČÜŅŗÖŠ£¬SO2ĘųĢåČ«²æ±»ĪüŹÕ£¬½«·“Ó¦ŗóµÄČÜŅŗŌŚæÕĘųÖŠŠ”ŠÄÕōøɣز»æ¼ĀĒĖįŹ½ŃĪµÄ·Ö½ā£©£¬µĆµ½²»³¬¹żĮ½ÖÖĪļÖŹµÄĪŽĖ®¾§Ģå26.8g”£Ķعż¼ĘĖćČ·¶ØĖłµĆ¾§ĢåµÄ³É·ÖÓėĪļÖŹµÄĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğÉĻŗ£ŹŠøßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
ÉĮŠææó(Ö÷ŅŖ³É·ŻĪŖZnS)ŹĒŗ¬ŠæÖ÷ŅŖæóĪļÖ®Ņ»£¬øßĪĀ¼ÓČČÉĮŠææóÉś³ÉZnOŗĶSO2”£ZnOÓĆÓŚŅ±Į¶½šŹōŠæ£¬SO2æÉÖĘŃĒĮņĖįŃĪ»ņĮņĖį”£¼ĘĖć»Ų“šĻĀĮŠĪŹĢā(±£Įō2Ī»Š”Źż)
£Ø1£©Č”1.56 gÉĮŠææóѳʷ£¬ŌŚæÕĘųÖŠøßĪĀ¼ÓČČ(ŌÓÖŹ²»·“Ó¦)£¬³ä·Ö·“Ó¦ŗó£¬ĄäČ“£¬µĆµ½²ŠĮō¹ĢĢåµÄÖŹĮæĪŖ1.32 g£¬ŃłĘ·ÖŠŗ¬Įņ»ÆŠæµÄÖŹĮæ·ÖŹżŹĒ_________”£
£Ø2£©Č”1.95 gŠæ¼ÓČėµ½12.00 mL 18.4 mol/LµÄÅØĮņĖįÖŠ(¼ŁÉčÉś³ÉµÄĘųĢåÖŠĪŽĒāĘų£¬ÅØĮņĖį²śÉśµ„Ņ»µÄ»¹Ō²śĪļ)£¬³ä·Ö·“Ó¦ŗ󣬊”ŠÄµŲ½«ČÜŅŗĻ”ŹĶµ½1000 mL£¬Č”³ö15.00 mL£¬ŅŌ·ÓĢŖĪŖÖøŹ¾¼Į£¬ÓĆ0.25 mol/LµÄNaOHČÜŅŗµĪ¶Ø£¬ŗÄÓĆNaOHČÜŅŗµÄĢå»żĪŖ21.70 mL”£Ķعż¼ĘĖćČ·¶ØÅØĮņĖį±»»¹ŌµÄ²śĪļŹĒ________”£
£Ø3£©Čō½«ZnSČÜÓŚĒæĖįæɲśÉśĮņ»ÆĒāĘųĢ唣ŌŚ120 oC”¢1 atmĻĀ£¬½«100 mLĮņ»ÆĒāŗĶŃõĘųµÄ»ģŗĻĘųĢåµćČ¼£¬»Öø“µ½ŌĄ“דĢ¬£¬²āµĆŹ£ÓąĘųĢåĪŖ70 mL£¬ĒóŌ»ģŗĻĘųĢåÖŠĮņ»ÆĒāµÄĢå»ż·ÖŹż”££Ø²»æ¼ĀĒĮņ»ÆĒāĘųĢå×ŌÉķŹÜČČ·Ö½ā£©
£Ø4£©½«±źæöĻĀ4.48 L SO2ĘųĢåĀżĀżĶØČė200 mLŅ»¶ØÅضČNaOHČÜŅŗÖŠ£¬SO2ĘųĢåČ«²æ±»ĪüŹÕ£¬½«·“Ó¦ŗóµÄČÜŅŗŌŚæÕĘųÖŠŠ”ŠÄÕōøɣز»æ¼ĀĒĖįŹ½ŃĪµÄ·Ö½ā£©£¬µĆµ½²»³¬¹żĮ½ÖÖĪļÖŹµÄĪŽĖ®¾§Ģå26.8g”£Ķعż¼ĘĖćČ·¶ØĖłµĆ¾§ĢåµÄ³É·ÖÓėĪļÖŹµÄĮ攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®1 mol ![]() ·Ö×ÓÖŠ£¬ŗ¬17”Į6.02”Į
·Ö×ÓÖŠ£¬ŗ¬17”Į6.02”Į![]() øö¹²ÓƵē×Ó¶Ō
øö¹²ÓƵē×Ó¶Ō
B£®10 mL 18.4 mol”¤![]() µÄÅØĮņĖįÓė90 mLÕōĮóĖ®»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ
µÄÅØĮņĖįÓė90 mLÕōĮóĖ®»ģŗĻ£¬ĖłµĆČÜŅŗÖŠ![]() =3£®68 mol”¤
=3£®68 mol”¤![]()
C£®25”ꏱ£¬ŌŚpH=4µÄ![]() ČÜŅŗÓėpH=10µÄ
ČÜŅŗÓėpH=10µÄ![]() ČÜŅŗÖŠ£¬Ė®µēĄė³öµÄ
ČÜŅŗÖŠ£¬Ė®µēĄė³öµÄ![]() Ē°Õß“óÓŚŗóÕß
Ē°Õß“óÓŚŗóÕß
D£®ŌŚ25 mL 0.1 mol”¤![]()
![]() ČÜŅŗÖŠ£¬µĪČė0.1 mol”¤
ČÜŅŗÖŠ£¬µĪČė0.1 mol”¤![]() µÄ
µÄ![]() ČÜŅŗÖĮ»ģŗĻČÜŅŗpH=7Ź±£¬ŌņµĪ¼Ó
ČÜŅŗÖĮ»ģŗĻČÜŅŗpH=7Ź±£¬ŌņµĪ¼Ó![]() ČÜŅŗµÄĢå»ż“óÓŚ25 mL
ČÜŅŗµÄĢå»ż“óÓŚ25 mL
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com