
 =1mol,由2Ag~Cl2~H2可知,理论上应提供标准状况下H2的体积为0.5mol×22.4L/mol=11.2L,故答案为:11.2L.
=1mol,由2Ag~Cl2~H2可知,理论上应提供标准状况下H2的体积为0.5mol×22.4L/mol=11.2L,故答案为:11.2L.

科目:高中化学 来源: 题型:
 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 1.1水的净化与污水处理练习卷(解析版) 题型:填空题
国务院强调,调水必须坚持“三先三后”的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的Mg2+、Al3+、Cu2+、Ag+。试分析回答下列问题。
(1)该废液中可能大量存在的一种阴离子是________(填字母代号)。
A. B.
B.
C.Cl- D.
(2)检测废液中铝元素的含量,需将其从废液样品中分离出来,所用的试剂可以是________溶液,铝元素发生变化的离子方程式是____________________________________________。
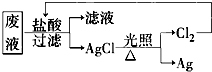
(3)为了回收废液中的金属银,某同学设计了如下方案:
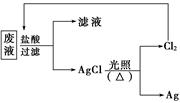
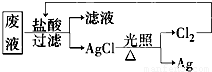
若依该方案获得Ag 108 g,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的H2的体积为____________。(Ag的相对原子质量为108)
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学必修二第四章 化学与可持续发展练习卷(解析版) 题型:填空题
(8分)(1)在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大原因。经检测某工厂废液中含有大量Mg2+、Al3+、Ag+,Fe3+、Ba2+。试分析回答下列问题:
①该废液中可能大量存在的一种阴离子是____(填序号)。
A.SO B.NO C.Cl- D.CO
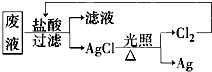
②为了充分利用资源和保护环境,今要回收废液中的金属银,请你设计一个回收实验方案,并写出有关离子反应方程式: ____________________________________________
________________________________________________________________________。
(2)节能减排是中国政府报告中的关键词。火力发电厂为了减少二氧化硫的排放,往往对煤炭进行脱硫处理,而脱硫的方法有多种,下面是一种常用的脱硫方法:
微生物脱硫技术:煤炭中的硫是以FeS2存在的,在水和空气存在的条件下,脱硫微生物起生物催化作用:
①2FeS2+7O2+2H2O  4H++2Fe2++4SO42—;
4H++2Fe2++4SO42—;
②4Fe2++O2+4H+ 4Fe3++2H2O;
4Fe3++2H2O;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2SO42—。
4H++2SO42—。
在微生物脱硫的反应中,FeS2最终被________氧化,转化为________(填化学式)而除去;反应③中若生成0.2 mol S,则转移的电子为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com