
| A�� | ��������ˮբ�ſ�����ӵ�Դ���������� | |
| B�� | ��ӦNH3��g��+HI��g���TNH4I��s���ڵ����¿��Է����У����H��0����S��0 | |
| C�� | �����£���0��lmol•L-1CH3COONa��Һ�еμ����ᣬ��Һ��ˮ�ĵ���̶����� | |
| D�� | �����½��еķ�Ӧ2NO2��g��?N2O4��g����ƽ��ʱ����С��������ٴ�ƽ��ʱ������ ����ɫ�ȵ�һ��ƽ��ʱ���� |
���� A����������������ӵ��������������������ֱ�Ϊ��������������������ԭ��Ӧ���ɷ�ֹ��������
B����Ӧ�Է����е��ж������ǡ�H-T��S��0���������ݷ�Ӧ����ʽ������
C��ˮ���ֵ���������ӡ����������ӣ�CH3COO-ˮ��ٽ�ˮ�ĵ��룬�μ����ᣬ���������������ˮ�ĵ��룻
D��ƽ���ƶ���Ӱ�첻����С�����Ӱ�죬��С����������ʵ�Ũ�Ⱦ�����������ɫ���
��� �⣺A������������������������ԭ��صĸ��������ױ���ʴ��������������������ԭ������ԭ���ԭ����Ӧ�ã����ñ������Ľ���������������ѡ��Ϊ�����������Һ����Ƭ�ĸ�ʴ��Ӧѡ��������õĽ������������ڵ���ڵ�·Ϊ��������Ϊ������������������������A��ȷ��
B����ӦNH3��g��+HI��g���TNH4I��s��������ӦΪ���������С�ķ�Ӧ����S��0����Ӧ�Է�������Ҫ�����H-T��S��0���ڵ����¿��Է����У����H��0����B����
C��CH3COONaΪǿ�������Σ���ȫ����������Ӻ���������ӣ����������ˮ�⣬�ٽ�ˮ�ĵ��룬������Һ�еμ����ᣬ�������������Ӻ���������ӽ������������ӣ�ͬʱ������Ũ����������ˮ�ĵ��룬������Һ�е�ˮ�ĵ���̶ȼ�С����C����
D����Ӧ2NO2��g��?N2O4��g����Ӧ�����������С�ķ�Ӧ���ﵽƽ�����С���������������ѹǿ��ƽ�������ƶ�������ѹǿ�����Ѹ�ټ�С��ƽ���ƶ��̶Ȳ��������С�����ĸı�����Ի��������ɫ�����D��ȷ��
��ѡAD��
���� ���⿼��绯ѧ��ʴ��������ѧ��Ӧ���еķ���������ʵĵ����Լ��ε�ˮ�⡢��ѧƽ��ȷ����֪ʶ��ע����շ�Ӧ�Է����е��ж����ݡ�Ӱ��ˮ�ĵ���ƽ�����صķ����ж��Լ�Ӱ�컯ѧƽ������أ�ע��֪ʶ�Ĺ��ɺ������ǽ���Ĺؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
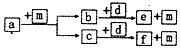 ������Ԫ��W��X��Y��Z��ԭ���������ε�����a��b��c��d��e��f������ЩԪ����ɵĻ����dΪ���ӻ������ṹ�л����Ǽ��Թ��ۼ���mΪԪ��Y�ĵ��ʣ�ͨ��Ϊ��ɫ��ζ�����壮�������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
������Ԫ��W��X��Y��Z��ԭ���������ε�����a��b��c��d��e��f������ЩԪ����ɵĻ����dΪ���ӻ������ṹ�л����Ǽ��Թ��ۼ���mΪԪ��Y�ĵ��ʣ�ͨ��Ϊ��ɫ��ζ�����壮�������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��W��X��Y��Z | |
| B�� | �����ӵĻ�ԭ�ԣ�Y��W | |
| C�� | ͼ�����ʵ�ת�����̾�Ϊ������ԭ��Ӧ | |
| D�� | aһ����W��X����Ԫ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu+HNO3��ϡ�� | B�� | N2+O2 | C�� | NH4Cl+O2 | D�� | NO2+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ��ʹ�ô������ܽ��÷�Ӧ�Ļ�� | |
| B�� | ��Ӧ��Ϊ���ȷ�Ӧ | |
| C�� | ��Ӧ�۽���ѧ��ת��Ϊ���� | |
| D�� | ��ӦCO��g��+H2O��g���TCO2��g��+H2��g������H=-82.4 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ��ˮ | B�� | NaOH��Һ | C�� | ���� | D�� | CO2��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��Mg��Al�Ľ��������μ��� | B�� | H2S��H2O��HF���ȶ������μ��� | ||
| C�� | Cl-��Br-��I- ��ԭ��������ǿ | D�� | Na��K��Rb��ԭ�Ӱ뾶�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
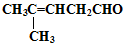 ���������ȩ�������õ��Լ���������Һ�������Ʊ�������ͭ��Һ������ѧ����ʽΪ
���������ȩ�������õ��Լ���������Һ�������Ʊ�������ͭ��Һ������ѧ����ʽΪ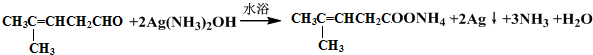 ��
��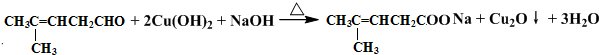 ��
��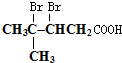 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
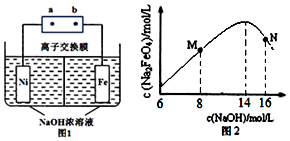
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com