
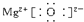 .
.分析 U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,Z的单质在X2中燃烧的产物可使品红溶液褪色,则Z为S,X为O,V的单质在X2中燃烧可生成VX和VX2两种气体,且原子序数小于X,则V为C,V、W、X 均可与U形成电子数相同的分子或离子,则U为H,W的原子序数介于V和X之间,所以W为N,Y的单质是一种金属,该金属与冷水反应缓慢,与沸水反应迅速,则Y为Mg,据此答题.
解答 解:U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,Z的单质在X2中燃烧的产物可使品红溶液褪色,则Z为S,X为O,V的单质在X2中燃烧可生成VX和VX2两种气体,且原子序数小于X,则V为C,V、W、X 均可与U形成电子数相同的分子或离子,则U为H,W的原子序数介于V和X之间,所以W为N,Y的单质是一种金属,该金属与冷水反应缓慢,与沸水反应迅速,则Y为Mg,
(1)W为N,W元素在周期表中的位置是第二周期第ⅤA族,氮气分子的结构式为N≡N,YX为MgO,它的电子式为 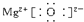 ,
,
故答案为为:第二周期第ⅤA族;N≡N;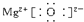 ;
;
(2)V为C,V元素形成的单质可能是金刚石或石墨,
故答案为:金刚石、石墨;
(3)V、W、X形成的10电子氢化物分别是CH4、NH3、H2O,元素蜚金属性越强,氢化物越稳定,由于非金属性O>N>C,所以稳定性由强到弱的顺序为H2O>NH3>CH4,
故答案为:H2O>NH3>CH4;
(4)SO2气体通人BaCl2和HNO3的混合溶液,发生氧化还原反应,生成白色沉淀BaSO4和无色气体NO,有关反应的离子方程式为 2H2O+3SO2+2NO3-+3Ba2+=3BaSO4+2NO+4H+,根据氧化还原反应中还原剂的还原性强于还原产物可知,由此可知NO和SO2还原性较强的是SO2,
故答案为:2H2O+3SO2+2NO3-+3Ba2+=3BaSO4+2NO+4H+;SO2.
点评 本题考查结构性质位置关系综合应用,题目较为综合,涉及分子结构与性质、电子式、氧化还原反应等,关键是正确推断元素,难度中等.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 乙烯制溴乙烷:CH2CH2+Br2→CH2BrCH2Br | |
| B. | 乙醇催化氧化:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3COH+2H2O | |
| C. | 苯与氢气加成: +3H2$\stackrel{Ni}{→}$ +3H2$\stackrel{Ni}{→}$ (环己烷) (环己烷) | |
| D. | 从海带中提取碘:H2O2+2I-+2H+=I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 条件 | 结论 |
| A | 若X原子半径X>Y | 原子序数:X<Y |
| B | 若最高价氧化物对应水化物酸性X>Y | 元素的电负性:X>Y |
| C | 若价电子数X>Y | 最高正价:X>Y |
| D | 若X、Y最外层电子数分别为1、7 | X、Y之间一定能形成离子键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=+890 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890 kJ•mol-1 | |
| D. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=-890 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 6:1 | B. | 2:1 | C. | 1:2 | D. | 9:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 可用溴水或FeCl3溶液鉴别X和Y | |
| B. | 反应物X与中间体Y互为同系物 | |
| C. | 普罗帕酮分子中有2个手性碳原子 | |
| D. | X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PbO2 为正极,被氧化 | |
| B. | 电解质溶液中 c(H+) 逐渐增大 | |
| C. | 电池电解质溶液的密度不断减小 | |
| D. | 该电池的负极反应式为:Pb-2e-═Pb2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com