
【题目】I.NO是第一个被发现的生命体系气体信号分子,具有舒张血管的功能。工业上可用“氨催化氧化法”生产NO,主要副产物为N2。请回答下列问题:
(1)以氨气、氧气为原料,在催化剂存在下生成NO和副产物N2的热化学方程式如下:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)
4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)
2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)![]() 2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
(2)某化学研究性学习小组模拟工业合成NO的反应。在1110K时,向一恒容密闭容器内充入1mol NH3和2.8mol O2,加入合适催化剂(催化剂的体积大小可忽略不计),保持温度不变,只发生反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①下列各项能说明反应已达到化学平衡状态的是_______。(填字母序号)
a.5c(NH3)=4c(O2)
b.N-H键的生成速率与O-H键的生成速率相等
c.混合气体的压强不变
d.混合气体的密度不变
②若其他条件不变,将容器改为恒容的绝热容器,在达到平衡后的体系温度下的化学平衡常数为K1,则K1_____K(填“>”、“<”或“=”)。
II.(3)某化学研究性学习小组模拟用CO和H2合成甲醇,其反应为:CO(g)+2H2(g) ![]() CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=_______,该温度下平衡常数K=_______。
III.(4)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
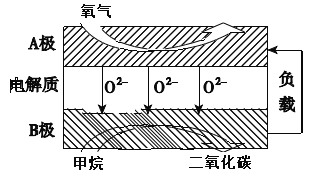
①B极上的电极反应式为_____________。
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到5.6 L(标准状况)气体时,消耗甲烷的体积为________L(标准状况下)。
【答案】 △H3=(△H1—△H2 )/2 b c < 0. 075 mol/(L﹒min) 3(mol/L)-2 (单位不作要求) CH4-8e-+4O2-=CO2+2H2O 2.8
【解析】
(1)由盖斯定律计算可得△H3;
(2)①根据化学平衡状态的特征分析,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化,注意选择的物理量应随反应进行发生变化,该物理量由变化到不变,说明到达平衡;
②该反应为放热反应,反应过程中反应温度升高,平衡向逆反应方向移动,化学平衡常数减小;
(3)依据表给数据建立三段式,通过化学反应速率公式和化学平衡常数公式计算化学反应速率和化学平衡常数;
(4)①由阴离子移动方向可知B为负极,负极发生氧化反应,甲烷被氧化生成二氧化碳和水;
②依据得失电子数目守恒计算消耗甲烷的体积。
(1)由盖斯定律可知,(①—②)/2得N2(g)+O2(g)![]() 2NO(g),则△H3=(△H1—△H2 )/2,故答案为:△H3=(△H1—△H2 )/2;
2NO(g),则△H3=(△H1—△H2 )/2,故答案为:△H3=(△H1—△H2 )/2;
(2)①a、5c(NH3)=4c(O2)与反应的初始物质的量以及反应的转化程度有关,不能确定是否达到平衡,错误;
b、N-H键的生成速率与O-H键的生成速率相等说明正逆反应速率相等,反应达到平衡状态,正确;
c、该反应是一个反应前后气体体积改变的化学反应,当反应达到平衡状态时,各物质的量不变,导致容器中压强不随时间的变化而改变,混合气体的压强不变能够说明反应达到平衡状态,正确;
d、容器是恒容的,无论反应是否达到平衡状态,混合物的质量始终不变,容器的体积不变,导致密度始终不变,混合气体的密度不变不能说明费用达到平衡,错误;
故选bc,故答案为:bc;
②该反应为放热反应,若其他条件不变,将容器改为恒容的绝热容器,反应过程中反应温度升高,平衡向逆反应方向移动,化学平衡常数减小,故答案为:<;
(3)由表中数据可知,20min时处于平衡状态,设CO的转化率为x,依据题意建立如下三段式:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始量(mol):2 4 0
变化量(mol):x 2x x
平衡量(mol):2-x 4-2x x
压强之比等于物质的量之比,则平衡时混合气体总物质的量为(2mol+4mol)×6.2MPa/12.4MPa=(6-2x)mol,解得x=1.5 mol,则反应消耗c(CO)=1.5mol/1L=1.5 mol/L,
以CO浓度变化表示的平均反应速率v(CO)=1.5 mol/L/20min=0.075mol/(L.min);化学平衡常数K=c(CH3OH)/c(CO)c2(H2)= 1.5 mol/L/0.5 mol/L×(1 mol/L)2=3(mol/L)-2,故答案为:0.075mol/(L.min);3(mol/L)-2;
(4)①由阴离子移动方向可知B为负极,负极发生氧化反应,甲烷被氧化生成二氧化碳和水,电极方程式为CH4+4O2--8e-=CO2+2H2O,故答案为:CH4+4O2--8e-=CO2+2H2O;
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到5.6L(标准状况)氧气时,反应转移1mol 电子,由得失电子数目守恒可知消耗甲烷的物质的量为0.125mol,则甲烷的体积为0.125mol×22.4mol/L=2.8L,故答案为:2.8。


科目:高中化学 来源: 题型:
【题目】通过溶解、过滤、蒸发等操作,可将下列各组固体混合物分离的是( )
A. 硝酸钠和氢氧化钠 B. 二氧化锰和氧化铜
C. 氯化钾和二氧化锰 D. 碳酸钾和氯化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列自然资源的开发利用中,不涉及化学变化的是:
①石油的分馏;②煤的干馏;③将石油催化裂解生产乙烯;④用铝热反应焊接钢轨;⑤用乙烯制取聚乙烯;⑥用铁矿石冶炼铁;⑦乙烯做植物生长调节剂和果实催熟剂;⑧用蒸馏法从海水制取淡水;⑨用食醋清除暖水瓶中的水垢;⑩将干冰放在通风处自然升华
A. ①②③④ B. ①②⑤⑦ C. ①⑧⑩ D. ①②⑥⑨ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 晶体中既含有离子键,又含有共价键
晶体中既含有离子键,又含有共价键
B.![]() 晶体是原子晶体,加热融化时需克服分子间作用力和共价键
晶体是原子晶体,加热融化时需克服分子间作用力和共价键
C.HCl、HBr、HI的热稳定性依次增强
D.化学键的被破坏的过程一定都涉及化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.常温常压下,一氧化二氯(Cl2O)为棕黄色气体。沸点为3.8℃,当温度高于42℃时,分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。将氯气和空气(不参与反应)按照体积比1:3混合后,通入含水量为8%(质量分数)的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。
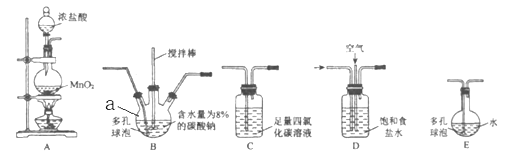
(1)仪器a的名称是 ________________。
(2)上述装置合理的连接顺序为 ___ →___ →___ → C →___ →(填装置下方的大写字母)。
(3)反应过程中装置B需要放在冷水中,其目的是________________________________。
(4)装置C的作用 __________________________________。
(5)制备Cl2O的化学方程式____________________________________________。
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点主要为_________________。
II.(7)探究NO与Na2O2反应的产物。
假设1:产物只有NaNO2;
假设2:__________;
假设3:产物为NaNO3和NaNO2的混合物。
为验证反应产物,该小组同学准确称取反应后的固体3.50 g,用煮沸并冷却后的蒸馏水配成100.00 mL溶液,取10.00 mL溶液于锥形瓶中,用0.200 0 mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液10 mL。滴定过程中发生反应的离子方程式为_______________,反应产物中NaNO2的质量分数为_________(保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①NaClO溶液;②Cu;③稀硫酸;④BaSO4;⑤乙醇;⑥SiO2;⑦乙烯;⑧熔融的KCl;⑨石墨;⑩冰醋酸。回答下列问题:
(1)上述物质中属于电解质的是______。(填写序号,以下同)
(2)上述物质中可以导电的是______。
(3)写出在催化剂存在条件下⑦转化为⑤的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将200mLH2SO4和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干燥、称量,得到46.6g白色沉淀。请计算:
(1)原溶液中c(SO42-)=______;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D是食品中的常见有机物,A是生物的主要供能物质。以A和水煤气(CO、H2)为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知E是CO和H2以物质的量之比1:2反应的产物,F为具有特殊香味、不易溶于水的油状液体。

请回答:
(1)有机物A的分子式______,有机物D中含有的官能团名称是______。
(2)B→C的反应类型是______,C的结构简式为______。
(3)B→C化学方程式是______。D+E→F的化学方程式______。
(4)下列说法不正确的是______。
A.有机物B与金属钠反应比水与金属钠反应要剧烈
B.除去F中含有D、E杂质可用NaOH溶液洗涤、分液
C.D和E反应生成F时,浓硫酸主要起强氧化剂作用
D.C在一定条件下可以与H2反应转化为B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属冶炼的叙述中,不正确的是( )
A.电解铝时,以氧化铝—冰晶石熔融液为电解质,也常加入少量CaF2帮助降低熔点
B.电解铝时阴极碳块需定期更换
C.可利用铝热反应从V2O5中冶炼金属V
D.可用加热法从HgO中冶炼Hg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com