


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 过量NH3 |
| Ⅰ |
| 过量CO2 |
| Ⅱ |
溶解度(g) 温度(℃) | NH4Cl | NH4HCO3 | NaHCO3 | NaCl | Na2CO3 | (NH4)2CO3 |
| 20 | 28.7 | 21.7 | 9.6 | 31.5 | 21.5 | 100 |
| 30 | 41.1 | 27.0 | 11.1 | 36.3 | 39.7 | >100 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HX可能是强酸 |
| B、NaX水溶液的碱性弱于NaY水溶液的碱性 |
| C、HX一定是弱酸 |
| D、反应过程中二者生成H2的速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、2c(H+)=c(CH3COO-)-c(CH3COOH) |
| D、c(CH3COOH)+c(CH3COO-)=0.01mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
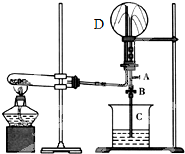 如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;
如图为实验室制取NH3且检验其某一性质的实验装置图.完成下列问题;查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH相等的①NH4Cl ②(NH4) 2SO4③NH4HSO4的溶液中,c(NH4+)大小:①>②>③ |
| B、向1.00L0.3mol?L-l的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中:3c (Na+)=2[c(HCO3-)+C (CO32-)+c(H2CO3)] |
| C、浓度均为0.1 mol?L-1的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)-c (CH3COOH)=c (H+)-c(OH-) |
| D、常温下,在l0mL pH=12的氢氧化钠溶液中加入pH=2的HA酸至pH刚好等于7,所得溶液体积V(总)≤20mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com