
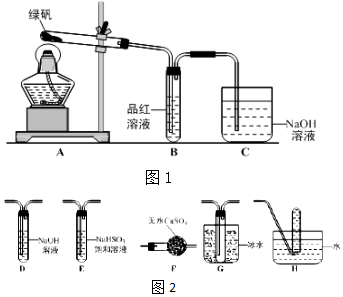
分析 (1)二氧化硫能使品红溶液褪色,二氧化硫污染空气,不能直接排放至空气中;
(2)根据题意SO3氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红分析;
(3)检验绿矾分解气态产物,由A分解绿矾,经F干燥,二氧化硫三氧化硫均能漂白品红,故先检验三氧化硫并与二氧化硫分离,三氧化硫熔沸点低,故连接G装置冷凝三氧化硫,由装置B检验二氧化硫,经过装置D除去二氧化硫,连接装置H,收集氧气,利用氧气的助燃性检验氧气;
(4)根据三价铁离子使KSCN溶液显红色分析.
解答 解:(1)甲组由此得出绿矾的分解产物中含有SO2,装置B为品红,二氧化硫有漂白性,故装置B中褪色;二氧化硫污染环境,用氢氧化钠吸收;
故答案为:品红溶液褪色;吸收尾气,防止SO2(SO3)等气体扩散到空气中污染环境;
(2)根据题意SO3氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红,三氧化硫的漂白不可恢复,乙对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中肯定有三氧化硫,未对二氧化硫检验,故可能含有二氧化硫;
故答案为:BC;
(3)①检验绿矾分解气态产物,由A分解绿矾,经F干燥,二氧化硫三氧化硫均能漂白品红,故先检验三氧化硫并与二氧化硫分离,三氧化硫熔沸点低,故连接G装置冷凝三氧化硫,由装置B检验二氧化硫,经过装置D除去二氧化硫,连接装置H,检验氧气;
故答案为:AFGBDH;
②氧气收集在H中,利用氧气支持燃烧检验,方法为:把H中的导管移出水面,撤走酒精灯,用姆指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;
故答案为:把H中的导管移出水面,撤走酒精灯,用姆指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;
(4)三价铁使KSCN溶液显红色,为证明绿矾分解产物中含有三价铁,则应用药匙取用分解产物于试管中,加盐酸溶解,再用胶头滴管向其中滴入KSCN溶液,若变红,则含有三价铁离子;
故答案为:药匙;盐酸,KSCN溶液.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、根据实验目的及物质的性质进行排列顺、实验基本操作能力及实验方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:解答题
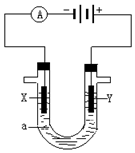 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.
人们习惯上把电解饱和食盐水的工业叫做氯碱工业.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
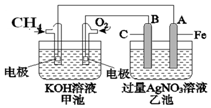 如图是一个化学过程的示意图.请回答下列问题:
如图是一个化学过程的示意图.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为负极,二氧化锰为正极 | |
| B. | 锌为正极,二氧化锰为负极 | |
| C. | 工作时电子由二氧化锰经外电路流向锌极 | |
| D. | 锌电极发生还原反应,二氧化锰发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡向正反应方向移动 | B. | 平衡将向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 容器内气体的密度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 序号 | 加热前的质量 | 加热后的质量 | 失水质量 | 结晶水的值 | |
| m0(容器) | m1(容器+晶体) | m2(容器+无水硫酸铜) | |||
| 1 | 35.503g | 35.685g | 35.620g | ①0.065 | ②4.9 |
| 2 | 35.503g | 35.663g | 35.606g | ③0.057 | ④3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,2-二甲基丙烷也称新戊烷 | |
| B. | 由乙烯生成乙醇属于加成反应 | |
| C. | 分子式为C5H11Cl的有机物共有8种(不含立体异构) | |
| D. | 所有的糖类、油脂、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠熔化时离子键被破坏 | |
| B. | 二氧化硅融化和干冰气化所破坏的作用力不相同 | |
| C. | H2SO4、CCl4、NH3均属于共价化合物 | |
| D. | HBr比HCl的热稳定性差说明HBr的分子间作用力比HCl弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com