
分析 (1)水在催化剂和激光条件下分解,吸收能量;
(2)氢氧燃料电池是将化学能转变为电能的装置,工作时,通入氢气的一极为电池的负极,发生氧化反应,通入氧气的一极为电池的正极,发生还原反应;
(3)A.储氢释氢是化学变化,化学变化中一定伴随能量变化;
B.储氢过程中C元素的化合价由+4降低为+2;
C.NaHCO3晶体中HCO3-中含有共价键,HCOONa晶体中HCOO-中含有共价键;
D.气体体积与温度和压强有关.
解答 解:(1)水在催化剂和激光条件下分解,吸收能量,为吸热反应,故答案为:吸热;
(2)负极通入氢气,氢气被氧化,电极方程式为2H2+4OH--4e-═4H2O(或H2+2OH--2e-═2H2O),总反应为2H2+O2═2H2O,电解质溶液体积增大,氢氧化钠浓度减小,则pH减小,
故答案为:2H2+4OH--4e-═4H2O(或H2+2OH--2e-═2H2O);减小;
(3)A.储氢、释氢过程都是化学变化,伴随之化学键的断裂和形成,则化学变化中一定伴随能量变化,故A错误;
B.储氢过程中C元素的化合价由+4降低为+2,NaHCO3被还原,故B错误;
C.NaHCO3晶体是离子晶体,由Na+与HCO3-构成,HCO3-中含有共价键,HCOONa晶体是离子晶体,由Na+与HCOO-构成,HCOO-中含有共价键,故C正确;
D.释氢过程中,每消耗0.1molH2O放出0.1mol的H2,只有在标准状况下0.1mol的H2为2.24L,该题未指明在标准状况下,所以0.1mol的H2不一定为2.24L,故D错误.
故答案为:C.
点评 本题以储氢方法为载体考查了氧化还原反应、化学反应中能量变化、化学键、气体摩尔体积的应用条件等,为高频考点,题目综合性较强,平时注意基础知识的全面掌握,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 为了使火腿肠颜色更鲜红,可多加一些亚硝酸钠 | |
| B. | 为了使婴儿对食品有浓厚兴趣,我们可以在婴儿食品中加少量着色剂 | |
| C. | 食盐加碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿 | |
| D. | 味精能增加食品的鲜味,促进食欲,炒菜时应该多放一点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
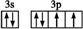 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
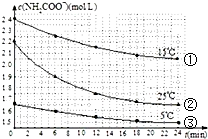 已知氨基甲酸铵发生的水解反应为:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,某研究小组得到c(NH2COO-)随时间变化曲线如图所示.下列有关说法一定正确的是( )
已知氨基甲酸铵发生的水解反应为:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,某研究小组得到c(NH2COO-)随时间变化曲线如图所示.下列有关说法一定正确的是( )| A. | 对比①与③,可知浓度越大水解速率越快 | |
| B. | 对比①与②,可知温度越高水解速率越快 | |
| C. | 加水稀释,平衡向正反应方向移动,K值增大 | |
| D. | 氨基甲酸铵在碱性条件下比在酸性条件下水解程度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学反应 | 平衡 常数 | 温度/℃ | ||
| 500 | 700 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 1.70 | 2.52 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | |||
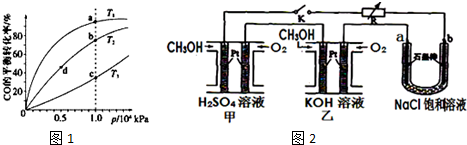
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
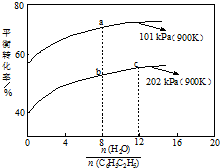 苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:
苯乙烯(C8H8)是生产各种塑料的重要单体,其制备原理是:| A. | a点转化率为75%,若起始向1 L恒容容器中充入1 mol 乙苯,则平衡常数为2.25 | |
| B. | b点转化率为50%,则混合气体中苯乙烯的体积分数为$\frac{1}{19}$ | |
| C. | 恒容时加入稀释剂能减小C8H10 (g)平衡转化率 | |
| D. | b点和c点温度和压强相同,所以反应速率也相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用过滤分离溶液和胶体 | |
| B. | 用渗析法可以除去溶液中的胶体粒子 | |
| C. | 向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 | |
| D. | 向Fe(OH)3胶体中加入足量稀盐酸后,依然有丁达尔效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com