
已知:2A(g)+3B(g) 2C(g)+zD(g),现将2mol A与3mol B混合于2 L的恒容密闭容器中,若反应进行2 s,A的转化率为40%,测得v(D)=0.2 mol·L-1·S-1,下列有关该反应的说法错误的是( )
2C(g)+zD(g),现将2mol A与3mol B混合于2 L的恒容密闭容器中,若反应进行2 s,A的转化率为40%,测得v(D)=0.2 mol·L-1·S-1,下列有关该反应的说法错误的是( )
A.z=2
B.2s末,反应物B的浓度为0.9mol·L-1
C.若反应再经2s达平衡,则平衡时生 成物D的浓度为0.8mol·L-1
成物D的浓度为0.8mol·L-1
D.反应达平衡时,反应物A、B的分子数之比为2:3
科目:高中化学 来源:2015-2016学年甘肃省高一下期末化学试卷(解析版) 题型:选择题
苯环结构中,不存在单双键交替结构,可以作为证据的事实是
①苯不能使酸性KMnO4溶液褪色;
②苯中碳碳键的键长均相等;
③苯能在一定条件下跟H2加成生成环己烷;
④经实验测得邻二甲苯(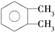 )仅一种结构;
)仅一种结构;
⑤苯在FeBr3存在的条件下同液溴可发生取代反应,但不能因化学变化而使溴水褪色。
A. ③④⑤ B. ①③④ . C. ①②④⑤ D. ①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷(解析版) 题型:填空题
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。
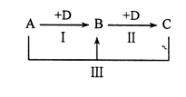
(1)若A为强碱溶液,其焰色反应显黄色,C常用作食品添加剂,请回答下列问题:
①物质的量浓度相同的B、C水溶液的pH前者 (填大于或小于)后者。
②反应Ⅲ的离子方程式是 。
③现有B和C的固体混合物ag,加热至质量不再改变时剩余固体为bg,则B的质量分数为 。
(2)若C、D均为金属单质,向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则:
①反应III的离子方程式是 。
②实验室中储存B溶液时应加入________。
③检验溶液A中金属阳离子的方法是 。
(3)若D为强电解质、B为难溶于水的沉淀,
①则A和C反应的离子方程式________________
②符合条件的D物质可能是下列物质中的________(填序号)。
a.硫酸
b.醋酸
c.氢氧化钠
d.氨水
e.氯化钡
f.硝酸镁
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷(解析版) 题型:选择题
某化学兴趣小组设计了下列四个实验装置,试图通过观察实验现象说明CO2与NaOH溶液发生了反应。其中无法达到实验目的的是( )
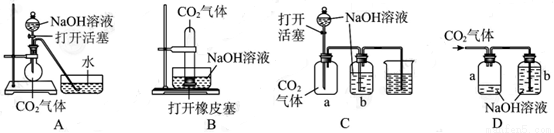
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:填空题
标准状况下将1.92 g铜粉投入100mL浓HNO3中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混合气体1.12 L(标况下测定),假设溶液体积不变,请回答下列问题:
(1)反应后生成的硝酸铜溶液的浓度为 mol/L;
(2)被还原的硝酸的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:选择题
下列与有机物的结构、性质有关的说法正确的是( )
A.C5H12属于烷烃且有2种同分异构体
B.乙烯、氯乙烯、甲苯分子中的所有原子均共平面
C.C4H10与Cl2在光照条件下反应,可生成4种一氯代烃
D.苯分子中不含碳碳双键,所以不能发生加成反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:选择题
下列关于常见有机物的说法正确的是( )
A.乙醇、乙酸和乙烯均能使酸性KMnO4溶液褪色
B.乙醇、乙酸和苯均能发生取代反应
C.可用NaCl溶液除去乙酸乙酯中残留的乙酸
D.苯与溴水在催化剂作用下反应可生成溴苯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下期末化学试卷(解析版) 题型:填空题
(1)对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。现有下列六种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2,按照不同的分类标准,它们中有一种物质与其他五种有明显的不同,请找出这种物质,并写出分类的依据(写出两 种分类方法)。
种分类方法)。
①_____________________________________ ;
②______________________________________。
(2) CH3OH 可与HNO3反应,将HNO3还原成N2,若该反应消耗3.2gCH3OH转移0.6 m ol电子,请写出其化学方程式: 。
ol电子,请写出其化学方程式: 。
(3)在SnCl2溶液中滴入酸性KMnO4溶液,生成Sn4+,有Cl2逸出,写出该反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-===Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2 mol电子,锌的质量理论上减少6.5 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com