
【题目】下列各组物质与其分类和用途的关系正确的是
A. 镁——单质——照明弹
B. 氧化钠——氧化物——供氧剂
C. 小苏打——碱——发酵粉主要成分
D. 水玻璃溶质——酸——防火材料
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】实验测知 K3C60 熔融状态下能导电,关于 K3C60 的分析错误的是
A.是强电解质B.存在两种作用力
C.是离子晶体D.阴阳离子个数比为 20∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知

A. X、Y、Z中最简单氢化物稳定性最弱的是Y
B. 元素氧化物对应水化物的酸性:Z>Y
C. 元素形成的单核阴离子还原性:X>Y
D. Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M,N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 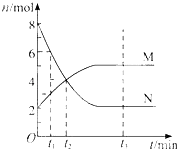
A.反应的化学方程式为:2MN
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是

A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7
B. 化合物F中含有共价键和离子键
C. 0.1molB与足量C完全反应共转移电子数为0.2NA
D. Z元素的最高正价为+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积固定的某密闭容器中发生反应N2+3H2![]() 2NH3。在10s内N2的浓度由5 mol·L-1降至4 mol·L-1,下列说法正确的是( )
2NH3。在10s内N2的浓度由5 mol·L-1降至4 mol·L-1,下列说法正确的是( )
A. 用NH3表示的化学反应速率为0.1 mol·L-1·s-1
B. 使用合适的催化剂,可以加快该反应的速率
C. 增加H2的浓度或降低温度都会加快该反应速率
D. 反应足够长时间,N2、H2中至少有一种物质浓度降为零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1H < 0(I)
NaNO3(s)+ClNO(g) K1H < 0(I)
2NO(g)+Cl2(g)![]() 2ClNO(g) K2H < 0(II)
2ClNO(g) K2H < 0(II)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______(用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=8.0×10-3molL-1min-1,回答下列问题
①平衡后n(Cl2)=__________mol,
②NO的转化率а1=_______。
③其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2________а1(填“>”“<”或“=”),平衡常数K2___________(填“增大”“减小”或“不变”)。
④若要使K2减小,可采用的措施是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是金属镁和卤素反应的能量变化图(反应物和生成物均为298 K时的稳定状态)。下列选项中不正确的是( )
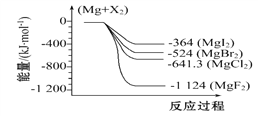
A. Mg与F2反应的ΔS<0 B. MgF2(s)+Br2(l)MgBr2(s)+F2(g)ΔH=+600 kJ·mol-1
C. MgBr2与Cl2反应的ΔH<0 D. 化合物的热稳定顺序:MgI2>MgBr2>MgCl2>MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料。以CO2为原料可合成多种物质。
(1)利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为:
①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol1
反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H= ____。
(2)在一定温度下,向2L固定容积的密闭容器中通入2 mol CO2和6 mol H2发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
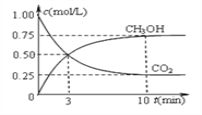
①前10 min内的平均反应速率υ(H2)=____ mol∕(L·min)。
②能说明该反应已达平衡状态的是____。
A.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
B.混合气体的平均摩尔质量保持不变
C.CH3OH的体积分数在混合气体中保持不变
D.混合气体的密度不随时间变化
③下列措施能使n(CH3OH) ∕n(CO2) 增大的是____。
A.升高温度 B.恒温恒容充入He(g)
C.使用高效催化剂 D.恒温恒容下,再充入1mol CO2、3mol H2
④该温度下的平衡常数K=____(L∕mol)2。
(3)用100mL 0.25 mol∕L Na2CO3溶液吸收标准状况下336mL的CO2气体(溶液体积变化忽略不计),所得溶液中:c(HCO3)+c(CO32)+c(H2CO3)=____ mol∕L(填数字)。
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。

① b电极的名称是____。
② 请写出电解时生成乙烯的电极反应式____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com