
 在实验室中用浓盐酸与MnO2共热制取Cl2.
在实验室中用浓盐酸与MnO2共热制取Cl2.分析 (1)周期序数=电子层数,主族元素最外层电子数等于族序数,也等于最高正化合价;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯化锰、氯气和水,注意浓盐酸在离子方程式中应该写成离子形式;
(3)①根据氯气密度比空气大,不溶于饱和食盐水的特点收集;
②氯气和水反应的方程式:Cl2+H2O=HClO+HCl,氯水的成分:Cl2、HCl、H2O,H+、Cl-、ClO-、OH-,据此进行分析;
③可根据氯气与溴化钠的反应比较Cl2和Br2的氧化性,氯气易溶于四氯化碳,在四氯化碳中颜色呈橙色.
解答 解:(1)氯元素是17号元素有三个电子层,最外层7个电子,所以位置为第3周期第VⅡA族,
故答案为:第3周期第VⅡA族;
(2)二氧化锰与浓盐酸在加热条件下反应生成氯气,反应的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(3)①A.收集气体时,集气瓶不能用橡胶塞堵住,应用双孔橡胶塞,故A错误;
B.该装置收集的是密度小于空气的气体,而氯气密度大于空气,且氯气有毒不能直接排放,故B错误;
C.该装置收集比空气密度大的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D.氯气与氢氧化钠反应,得不到氯气,故D错误;
故答案为:C;
②氯气和水反应的方程式:Cl2+H2O=HClO+HCl,氯水的成分:Cl2、HCl、H2O,H+、Cl-、ClO-、OH-,具有氧化性的含氯粒子是:Cl2、HClO、ClO-,
故答案为:Cl2、HClO、ClO-;
③该同学设计实验比较Cl2和Br2的氧化性,操作与现象是:取适量NaBr溶液于试管中,用胶头滴管向试管中滴加适量的新制氯水,然后再加入CCl4,振荡静置,观察现象,此时液体分层,下层溶液呈橙红色,
故答案为:振荡静置,观察现象,此时液体分层,下层溶液呈橙红色.
点评 本题考查了氯气的实验室制法和氯水的成分和性质,为高频考点,侧重于学生的分析、实验能力的考查,题目难度不大,注意相关基础知识的积累.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
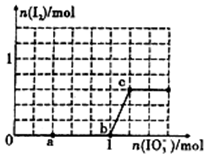 已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加人KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加人KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A. | 0-a段发生反应:3 HSO3-+IO3-═3SO42-+I-+3H+ | |
| B. | a~b段共消耗NaHSO3的物质的量为1.8mol | |
| C. | b~c段反应:氧化产物为I2 | |
| D. | 当溶液中I-与I2的物质的量之比为5:1时,加入的KIO3为1.lmol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3溶液、CCl4、BaCl2溶液 | B. | Na2SO3溶液、FeCl3溶液、H2S溶液 | ||
| C. | SO2气体、KOH溶液、镁粉 | D. | NaOH溶液、CO气体、石蕊溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C 元素的相对分子质量是 12,则 1mol C 的质量为 12g/mol | |
| B. | 1mol Cl2 的体积为 22.4L | |
| C. | 1mol CO2 中含有 3 个原子 | |
| D. | 已知 NaOH 溶液的物质的量浓度为 0.5mol/L,则 2L 该溶液中含 NaOH 1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把100mL3mol•L-1的H2SO4跟100mL水混合,硫酸的物质的量浓度变为1.5 mol•L-1 | |
| B. | 把200mL3mol•L-1的BaCl2溶液跟100mL3mol•L-1的KCl溶液混合后,溶液中的c(Cl- )仍然是3mol•L-1 | |
| C. | 把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10% | |
| D. | 1 L 水中溶解 0.2 mol 硝酸钾,即可配得 0.2 mol/L 硝酸钾溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com