
| A.V1=10V2 | B.V1>10V2 | C.V1<10V2 | D.V2>10V1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.盐酸 | B.氯化钾溶液 | C.硝酸银溶液 | D.硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
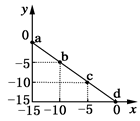
| A.该温度高于25℃ |
| B.图中a点溶液呈碱性 |
| C.该温度下,0.01 mol·L-1的HCl溶液的pH=2 |
| D.该温度下,0.01 mol·L-1的NaOH溶液的pH=12 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将pH=3的醋酸稀释后,溶液中所有离子的浓度均降低 |
| B.在纯水中加入少量NaOH或醋酸钠均可抑制水的电离 |
| C.常温下,将pH=3的盐酸和pH=11的氨水等体积混合,溶液的pH>7 |
| D.用标准NaOH溶液滴定醋酸至刚好完全反应时,溶液中C(Na+)=C(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH = 8的某电解质溶液 | B.c(OH-)>1×10-7mol/L |
| C.溶液中含有OH-. | D.溶液中c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 之比为2:1
之比为2:1 ;b.
;b. ;c.
;c. ;d.
;d. 。其溶液物质的量浓度由小到大顺序为d、b、c、a
。其溶液物质的量浓度由小到大顺序为d、b、c、a 溶液中滴加NaOH溶液至溶液pH=7,则
溶液中滴加NaOH溶液至溶液pH=7,则

| A.③⑤⑥ | B.③④⑥ | C.④⑤⑥ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤⑥⑦⑧ | B.①②③④⑦⑤⑥⑧ |
| C.②①③④⑦⑤⑥⑧ | D.②①③④⑤⑥⑦⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com