
气态氯化铝分子以双聚形式存在,其结构式如图所示:
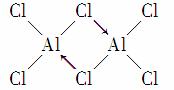
其中Cl→Al表示氯原子提供了一对电子与铝原子共享。又已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它只是一元酸。可以用硼酸在水溶液中的电离平衡解释它只是一元酸的原因,请写出下面这个化学方程式右端的两种离子的表达式:
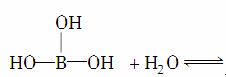 ____________________+________。
____________________+________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.c(H+)/c(OH-)=1×1014的溶液:Fe2+、K+、HSO 、ClO-
、ClO-
B.0.1 mol·L-1 FeCl3溶液:NH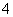 、H+、I-、SCN-
、H+、I-、SCN-
C.0.1 mol·L-1 Na2CO3溶液:K+、Ca2+、HCO 、SO
、SO
D.使酚酞变红色的溶液:Na+、Ba2+、NO 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2 800 | 2 050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是______________________________
________________________________________________________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是__________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关离子键的叙述中正确的是( )
A.离子化合物中只含有离子键
B.共价化合物中可能含离子键
C.含离子键的化合物不一定为离子化合物
D.共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
在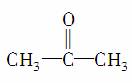 分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为( )
分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为( )
A.sp2杂化;sp2杂化 B.sp3杂化;sp3杂化
C.sp2杂化;sp3杂化 D.sp1杂化;sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
已知次氯酸分子的结构式为H—O—Cl,下列有关说法不正确的是( )
A.O原子发生sp3杂化
B.O原子与H、Cl都形成σ键
C.该分子为直线形分子
D.该分子为极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
测定Na2S2O3·5H2O产品纯度
准确称取W g Na2S2O3·5H2O产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O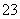 +I2===S4O
+I2===S4O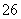 +2I-
+2I-

(5)滴定至终点时,溶液颜色的变化:___________________________________________。
(6)测定起始和终点的液面位置如图,则消耗碘的标准溶液体积为________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com