
分析 ①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l)△H2=-622kJ/mol
③H2O(l)=H2O(g)△H3=+44kJ•mol-1
依据盖斯定律:②×2-①+③×4计算焓变书写热化学方程式.
解答 解:①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(l)△H2=-622kJ/mol
③H2O(l)=H2O(g)△H3=+44kJ•mol-1
依据盖斯定律:②×2-①+③×4得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-622×2-67.7+44×4=-1135.7KJ/mol;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
点评 本题考查了热化学方程式的书写方法和盖斯定律的计算应用,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 相同条件下,每吸收10m3SO2就会放出5m3CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
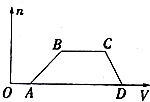 某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的几种物质,往该溶液中逐渐加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示.回答下列问题:
某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的几种物质,往该溶液中逐渐加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L盐酸和0.1mol/L醋酸分别与0.2mol/L氢氧化钠溶液反应的速率相同 | |
| B. | 0.1mol/L盐酸和0.1mol/L硝酸分别与大小相同的大理石反应的速率相同 | |
| C. | 铝和铁分别与0.1mol/L硫酸的反应速率相同 | |
| D. | 大理石块与大理石粉末分别与0.1mol/L盐酸反应的速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制CuSO4时先将Cu氧化成CuO后再与稀硫酸反应 | |
| B. | 采用银作催化剂,乙烯和氧气制取环氧乙烷,原子利用率100% | |
| C. | 用乙醇代替汽油作汽车燃料 | |
| D. | 用稀硝酸和铜制取Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有质子的微粒一定有中子 | |
| B. | 通常所说的氢元素是指${\;}_{1}^{1}$H | |
| C. | 16O中的“16”表示氧元素的近似相对原子质量 | |
| D. | 根据反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O得到的Cl2,其相对分子质量为73.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com