
 2012年世界青年奥运会将在南京举办.保护环境,人人有责.
2012年世界青年奥运会将在南京举办.保护环境,人人有责.分析 ①纳入空气质量监测的是可吸入颗粒物、NO2、SO2等污染大气的物质,二氧化碳为无毒气体;
②明矾溶于水时电离出的铝离子水解生成氢氧化铝胶体,具有吸附性可以净水;氯气或二氧化氯具有强氧化性,可消毒杀菌;
③干冰在通常状况下干冰易升华的特点分析;
④CO、NO相互作用生成可参与大气循环的两种气体应为氮气和二氧化碳,配平即得化学方程式;
⑤如图所示的垃圾分类标志的含义是循环再生或回收.
解答 解:①PM2.5、NO2、SO2都是污染大气的物质,二氧化碳为无毒气体,故空气质量监测中,不需要监测的指标是CO2浓度,故答案为:D;
②明矾溶于水时电离出的铝离子水解生成氢氧化铝胶体,具有吸附性可以净水,故其作用是混凝剂;氯气或二氧化氯具有强氧化性,可消毒杀菌,
故答案为:混凝剂; 消毒杀菌;
③在常压下,-78℃时,二氧化碳气体凝结成固态二氧化碳,俗称干冰,在通常状况下干冰易升华,故B正确,
故答案为:B;
④CO、NO相互作用生成可参与大气循环的两种气体应为氮气和二氧化碳,故化学方程式为:2NO+2C$\frac{\underline{催化剂}}{△}$N2+2CO2,
故答案为:2NO+2CO $\frac{\underline{催化剂}}{△}$N2+2CO2;
⑤如图所示的垃圾分类标志的含义是循环再生或回收,故答案为:循环再生或回收.
点评 本题考查了常见生活环境的污染与防治问题,为高频考点,侧重于化学与生活、环境的考查,有利于培养学生良好的科学素养和树立环境保护意识,难度不大,注意积累.


科目:高中化学 来源: 题型:选择题
| A. | 可加入酸性KMnO4溶液鉴别苯、环己烯和己烷 | |
| B. | 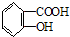 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 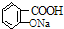 | |
| C. | 向卤代烃水解后的溶液中直接加入硝酸银溶液,可以确定卤代烃中的卤元素 | |
| D. | 利用盐析、过滤可将蛋白质和NaCl溶液分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
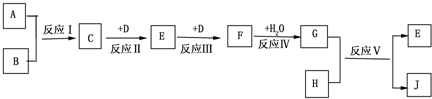
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 钢铁吸氧腐蚀时,负极反应式为2H2O+O2+4e-=4OH- | |
| C. | 镀锌铁皮的镀层损坏后,铁更容易被腐蚀 | |
| D. | 开发核能、风能和太阳能等新能源,都可降低碳排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 +CH3CH2OH$\stackrel{H+}{→}$
+CH3CH2OH$\stackrel{H+}{→}$ +H2O,
+H2O, ;
; ,则H的结构简式是
,则H的结构简式是 .高聚物L由H通过肽键连接而成,写出生成L的方程式n
.高聚物L由H通过肽键连接而成,写出生成L的方程式n →nH2O+
→nH2O+ (或
(或 ),.
),.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Y 表示的化学反应速率为0.005 mol/(L•s) | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若升高温度Y的转化率减小,则正反应为放热反应 | |
| D. | 达到平衡时,Y与Z的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性强弱:Na>Mg>Al | B. | 热稳定性:Na2CO3>NaHCO3 | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 酸性强弱:HIO4>HBrO4>HClO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com