
| A. | 参加反应的物质的性质是决定化学反应速率的主要因素 | |
| B. | 光是影响某些化学反应速率的外界条件之一 | |
| C. | 在给定条件下,当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| D. | 不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率 |
分析 影响化学反应速率的因素有内因和外因,物质的性质为内因,为影响化学反应速率的主要因素,外因有温度、浓度、压强、催化剂等,其中催化剂只改变反应速率,但不能概念反应的方向,当可逆反应达到平衡状态时,正逆反应速率相等,反应达到化学反应限度,此时各物质的浓度不再发生改变,但化学平衡为动态平衡,当外界条件发生变化时,平衡发生移动.以此解答该题.
解答 解:A.反应物的性质为决定化学反应速率的主要因素,如钠能和冷水反应,铜和热水也不反应,故A正确;
B.有些反应在光照条件下可发生,如HClO的分解,则光是影响某些化学反应速率的外界条件之一,故B正确;
C.当可逆反应达到平衡状态时,各物质的浓度不再发生改变,反应达到化学反应限度,故C正确;
D.对于固体或纯液体参加的反应,增大压强,反应速率不变,故D错误.
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点和常见题型,注意把握内因和外因的区别,特别是催化剂的性质,为该题考查的侧重点,注意相关基础知识的积累,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
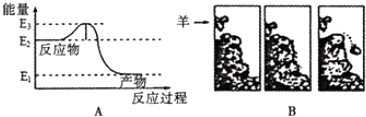
| A. | E2 | B. | E3 | C. | E2-E1 | D. | E3-E2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.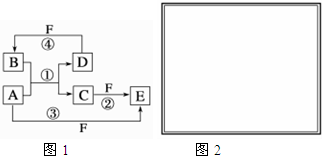
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
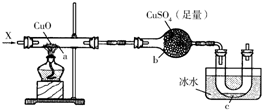 按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)
按照如图装置持续通入X气体或蒸气,可以看到a处有红色物质生成,b处变蓝,c处得到液体,(假设每个反应均完全)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;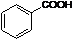 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新农村建设大量使用秸秆制取沼气,符合低碳理念 | |
| B. | 发霉的大米经过石蜡打磨后可以食用和出售 | |
| C. | 2014年西非国家爆发埃博拉病毒,双氧水、高锰酸钾溶液可以完全杀灭该病毒,其消毒原理和漂白粉消毒饮用水相同 | |
| D. | 卤水点豆腐、血液透析、静电除尘都是利用了胶体的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
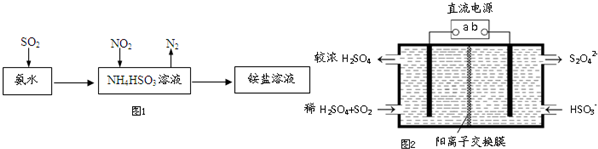
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1MgCl2溶液中的Mg2+数为nA | |
| B. | 1 mol Na2O2固体中含阴离子总数为2nA | |
| C. | 5 g质量分数为46%的乙醇溶液中,氢原子的总数为0.6 nA | |
| D. | 100 mL 12mol•L-1 浓盐酸与足量MnO2加热反应,转移电子数为1.2nA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com