
碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
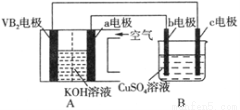
A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+
B.外电路中电子由c电极流向VB2电极
C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生
D.若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015内蒙古北方重工业集团三中高二下学期第一次月考化学试卷(解析版) 题型:填空题
(每空2分,共12分)已知:R-CH=CH-O-R′ R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4。与A相关的反应如下:
R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4。与A相关的反应如下:
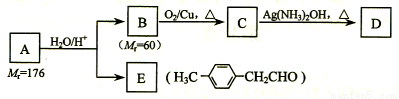
请回答下列问题:
(1)A的分子式为_________________。
(2)B的名称是___________________;A的结构简式为________________________。
(3)写出C → D反应的化学方程式:_______________________________________。
(4)写出两种同时符合下列条件的E的同分异构体的结构简式:
① 属于芳香醛;② 苯环上有两种不同环境的氢原子。________、___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
用铂作电极电解某种溶液,通电一段时间后,溶液的pH变小,且在阳极得到0.56L气体,阴极得到1.12L气体(两种气体体积均在相同条件下测定)。由此可知,该溶液可能是
A.CuSO4溶液 B.HBr溶液 C.NaCl溶液 D.硫酸溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省高一3月月考化学试卷(解析版) 题型:选择题
将足量CO2通入下列各溶液中,所含离子均还能大量存在的是
A.K+、OH-、Cl- B.Na+、K+、CO32-
C.Na+、HCO3-、SO42- D.Ba2+、AlO2-、NO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:填空题
(10分)金属镁是六方最密堆积,金属铜是面心立方最密堆积,下图分别给出它们的堆积状况和晶胞示意图,它们空间利用率相同,假定镁、铜原子均为刚性小球,已知球的半径分别为R1厘米、R2厘米,阿伏伽德罗常数NA
| (1)镁原子在二维空间的配位数为 |
(2)位于晶胞中部的鎂原子与离它最近两平面 (填“相离”或“相切”或”相交”) | |
(3)请用含R1、NA的数学式子表达金属镁的密度: g/cm3(根号带在分子上) | |
| (4)铜原子在三维空间的配位数为 |
(5)晶胞中面心上的六个铜原子构成的空间几何体名称为 | |
(6)请用含R2、NA的数学式子表达金属铜的密度: g/cm3(根号带在分子上) |
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。
已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)。下列说法正确的是

A.该温度下,Ksp (BaSO4 )=1.0×10-24
B.a点的Ksp (BaSO4 )小于b点的Ksp (BaSO4 )
C.d点表示的是该温度下BaSO4的不饱和溶液
D.加入BaCl2可以使溶液由 c点变到a点
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
下列关于杂化轨道的叙述中,不正确的是
A.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
B.分子中中心原子通过sp3杂化轨道成键时,该分子不一定为正四面体结构
C.杂化前后的轨道数不变,但轨道的形状发生了改变
D.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
查看答案和解析>>
科目:高中化学 来源:2014-2015学年新疆乌鲁木齐地区高三第二次诊断性测试化学试卷(解析版) 题型:填空题
选做(15分)【化学选修3:物质结构与性质】
原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E+核外各能层电子均已充满。请回答下列问题:
(1)X、Y、Z的第一电离能由小到大的顺序为 。(用元素符号表示)
(2)已知YZ2+ 与XQ2互为等电子体,则l mol YZ2+ 中含有π键数目为 。
(3)Z的气态氢化物沸点比Q的气态氢化物高得多,其原因是 。
(4)Y、Z与氢元素可形成化合物HYZ3,是实验室常用试剂。HYZ3分子中Y的杂化方式为 ,YZ3—的空间构型是 。
(5)E原子的价层电子排布式为 ;E有可变价态,它的基价态的离子与Z的阴离子形成晶体的晶胞如图所示。
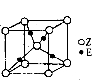
①该晶体的化学式为 ,Z的阴离子的配位数为 。
②Z的阴离子的堆积模型为 。
A.简单立方 B.六方最密 C.面心立方
③已知晶胞边长为apm,则晶胞的密度为 g cm—3(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省郑州市高三第二次质量预测理综化学试卷(解析版) 题型:选择题
25 ℃ 时,将某一元酸HA和NaOH溶液等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表:
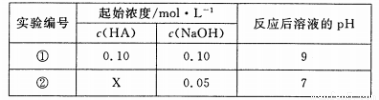
下列判断不正确的是
A、X>0.05
B、将实验①所得溶液加水稀释后,c(OHˉ )/c(A-)变大
C、实验①所得溶液c(A-)+c(HA)=0.10 mol·L-1
D、实验②所得溶液: c(Na+)+c(OH-)= c(A-)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com