
由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸.再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为 ( )
| A.0.1mol | B.大于或等于0.2mo1,小于0.3mol |
| C.等于0.2 mol | D.大于0.1mol小于0.3mol |
C
解析试题分析:8.96L气体的物质的量为8.96L÷22.4L/mol=0.4mol。NaOH溶液增重的质量就是燃烧生成的CO2的质量,即n(CO2)=26.4g÷44g/mol=0.6mol。已知1molCO,CH4都只能生成1molCO2,1molC2H6能生成2molCO2。因此设CO,CH4的物质的量之和为a,C2H6为b,则a+b=0.4mol、a+2b=0.6mol,解得b=0.2mol,答案选C。
考点:考查有机物燃烧的有关计算
点评:该题是高考中的常见题型,属于中等难度试题的考查,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确反应的原理,然后根据方程式并借助于守恒法列式计算即可。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
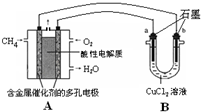 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源:朝阳区一模 题型:问答题
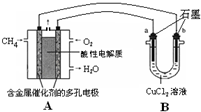
查看答案和解析>>
科目:高中化学 来源:2012年北京市朝阳区高考化学一模试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com