
 X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:
X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:分析 X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同,则A为H元素;Y原子核外有三个能级,且每个能级上容纳的电子数相同,原子核外电子排布式为1s22s22p2,则Y为C元素;W原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,则W为O元素;Z的原子序数介于碳、氧之间,则Z为N元素;Q元素的原子核外有26个运动状态完全不相同的电子,则Q为Fe.
解答 解:X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同,则A为H元素;Y原子核外有三个能级,且每个能级上容纳的电子数相同,原子核外电子排布式为1s22s22p2,则Y为C元素;W原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,则W为O元素;Z的原子序数介于碳、氧之间,则Z为N元素;Q元素的原子核外有26个运动状态完全不相同的电子,则Q为Fe.
(1)由H与O组成的含18个电子的分子为H2O2,结构式为H-O-O-H,故答案为:H-O-O-H;
(2)同周期随原子序数增大,元素第一电离能呈增大趋势,氮元素原子2p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能最大的是N>O>C;
Q元素的原子核外有26个运动状态完全不相同的电子,核外电子排布式为:1s22s22p63s23p63d64s2,
故答案为:N;1s22s22p63s23p63d64s2;
(3)CO32-离子中C原子孤电子对数=$\frac{4+2-2×3}{2}$=0、价层电子对数为3+0=3,离子的空间构型是 平面三角形,其中心原子的杂化轨道类型是sp2杂化,
故答案为:平面三角形;sp2;
(4)由Fe、N、O三种元素按照1:3:9的原子个数比可形成某离子化合物为Fe(NO3)3,铁离子水解溶液呈酸性,常温下测得该离子化合物的水溶液pH=2,则该溶液中由水电离产生的c(H+)为0.01mol/L,
故答案为:0.01mol/L;
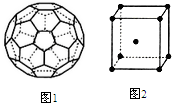
(5)碳元素的一种单质相对分子质量为720,则该分子为C60,分子构型为一个32面体,其中有12个五元环,20个六元环,每个碳周围有一个碳碳双键和两个碳碳单键,均为两个碳共用,所以每个碳实际占有的碳碳双键数为0.5,而每个双键中有一个π键,所以C60中π键的数目为60×0.5NA=30NA,
故答案为:30NA;
(6)Fe元素对应的单质在形成晶体时,采用图中堆积模型为体心立方堆积,即在立方体的中心有一个铁原子,与这个铁原子距离最近的原子位于立方体的8个顶点,所以铁的配位数为8;
晶胞中Fe原子数目为1+8×$\frac{1}{8}$=2,晶胞质量为2×$\frac{56}{{N}_{A}}$g,如果Fe的原子半径为 a cm,则立方体的边长为$\frac{4a}{\sqrt{3}}$cm,晶胞的体积为($\frac{4a}{\sqrt{3}}$cm)3,所以铁单质的密度表达式为2×$\frac{56}{{N}_{A}}$g÷($\frac{4a}{\sqrt{3}}$cm)3=$\frac{2×56}{{N}_{A}×(\frac{4a}{\sqrt{3}})3}$g/cm3,
故答案为:8;$\frac{2×56}{{N}_{A}×(\frac{4a}{\sqrt{3}})3}$.
点评 本题是对物质结构与性质的考查,涉及结构与位置关系、核外电子排布、电离能、杂化方式与空间构型判断、盐类水解、晶胞结构与计算,(5)(6)为易错点、难点,需要学生具备一定空间想象与计算能力,难度中等..


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{22.4b}{5a}$ | B. | $\frac{5a}{11.2b}$ | C. | $\frac{22.4a}{5b}$ | D. | $\frac{11.2b}{5a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质本身在常温常压下不一定导电 | |
| B. | 盐酸导电所以它是电解质 | |
| C. | 酸、碱、盐是电解质 | |
| D. | 氯化钠加入水中,在水分子作用下,形成自由移动的水合离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | A 探究铁发生吸 氧腐蚀 | B探究碳和硅金 属性的强弱 | C制取并收集氨气 | D制取并探究乙 炔的性质 |
实验方案 | 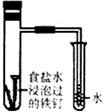 | 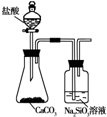 | 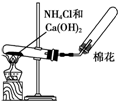 | 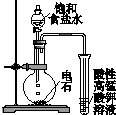 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K值不变,平衡可能移动 | |
| B. | 平衡向右移动时,K值不一定移动 | |
| C. | K值有变化,平衡一定移动 | |
| D. | 相同条件下,同一个反应的方程式的化学计量数增大2倍,K值也增大两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向正反应方向移动 | B. | 向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 不发生移动,但容器内压强增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
36.5gHCl气体溶解在1L水中(水的密度近似为1g/cm3), 所得溶液的密度为ρg/ml,质量分数为ω,物质的量浓度为c mol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是
A.所得溶液的物质的量浓度为1mol/L
B.所得溶液中含有NA个HCl分子
C.36.5gHCl气体占有的体积为22.4L
D.所得溶液的质量分数:ω=36.5c/(1000ρ)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
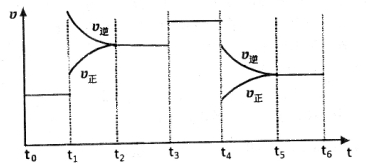
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com