
����Ŀ�����¶ȸ��� 500 K ʱ����ѧ�ҳɹ����ö�����̼�������ϳ����Ҵ������ڽ��ܼ��š�����̼�ŷŷ�������ش����塣
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ________________����ƽ�ⳣ������ʽΪK��________��
(2)�ں����ܱ������У��ж�������Ӧ�ﵽƽ��״̬��������________��
a����ϵѹǿ���ٸı� b��H2��Ũ�Ȳ��ٸı� c��������ܶȲ���ʱ��ı� d����λʱ�������� H2�� CO2�����ʵ���֮��Ϊ 3��1
(3)��֪��1 g ������ȫȼ������Һ̬ˮ���ų� 143 kJ ������23 g �Ҵ���ȫȼ������Һ̬ˮ�Ͷ�����̼���ų� 650 kJ ���������������Ҵ���ȼ���ȵı�ֵΪ________��(Ҫ��������ֵ)
(4)��һ��ѹǿ�£������ CO2��ȡ CH3CH2OH ��ʵ�������У���ʼͶ�ϱȡ��¶��� CO2��ת���ʵĹ�ϵ��ͼ��ʾ������ͼ������

�ٽ����¶ȣ�ƽ����________�����ƶ���
���� 700 K����ʼͶ�ϱ� n(H2)/n(CO2)��1.5 ʱ��H2��ת����Ϊ________��
���� 500 K����ʼͶ�ϱ�n(H2)/n(CO2)��2 ʱ�� �ﵽƽ��� H2��Ũ��Ϊa mol��L��1����ﵽƽ��ʱ CH3CH2OH ��Ũ��Ϊ________��
���𰸡�2CO2 +6H2![]() C2H5OH+3H2O c(C2H5OH)��c3(H2O)/[c6(H2)��c2(CO2)] ab 0.22 ����Ӧ 40% 1.5a mol/L
C2H5OH+3H2O c(C2H5OH)��c3(H2O)/[c6(H2)��c2(CO2)] ab 0.22 ����Ӧ 40% 1.5a mol/L
��������
(1)���ݶ�����̼�������ڸ���500Kʱ�ϳ����Ҵ���ԭ���غ���д��ѧ����ʽ����ѧƽ�ⳣ��Ϊ������Ũ�ȵĻ�ѧ���������ݵij˻������Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻��ı�ֵ������
(2)��һ�������£������淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ������Ҳ���䣬�������ʾ�Ϊ���壬���ں���״̬��������ܶȺ�Ϊ��ֵ�����ݻ�ѧ����ʽ��֪���κε�λʱ��������H2��CO2�����ʵ���֮�Ⱦ�Ϊ3:1���Դ˷�����
(3)������25����101kPaʱ��lmolij������ȫȼ��ʱ�����ȶ�����ķ�Ӧ�ȣ���Ϊ�����ʵ�ȼ�������ֱ�д���������Ҵ�ȼ�յ��Ȼ�ѧ����ʽ�������м�����
(4)����ͼ��֪��������ΪͶ�ϱȣ�������ΪCO2��ת���ʣ�����Ϊ�����ߣ�����ͬͶ�ϱ�ʱ�¶ȵͶ�Ӧ��CO2��ת���ʴ��Դ˷�����������ͼ��֪����700K����ʼͶ�ϱ�n(H2)/n(CO2)=1.5ʱ��������̼ת����Ϊ20%����CO2��H2����ʼ���ʵ����ֱ�Ϊ1mol��1.5mol��ת���Ķ�����̼Ϊ0.2mol�����ݻ�ѧ����ʽ��֪ת��������Ϊ0.6mol����������H2��ת���ʣ�������ʼʱc(CO2)=xmol��L-1������ʼʱc(H2)=2xmol��L-1����������ʽ�������
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ��2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK=c(C2H5OH)��c3(H2O)/[c6(H2)��c2(CO2)]��
CH3CH2OH(g)+3H2O(g)���÷�Ӧ��ƽ�ⳣ������ʽΪK=c(C2H5OH)��c3(H2O)/[c6(H2)��c2(CO2)]��
(2)a���÷�ӦΪ�����������С�Ļ�ѧ��Ӧ������ϵ��ѹǿ���ٸı�ʱ����Ӧ�ﵽƽ��״̬����a����������
b��H2��Ũ�Ȳ��ٸı䣬˵����Ӧ�ﵽƽ��״̬����b����������
c��������500Kʱ���������ʾ�Ϊ���壬���ں���״̬��������ܶȺ�Ϊ��ֵ���ܶȲ��䲻��˵����Ӧ�ﵽƽ��״̬����c������������
d�����ݻ�ѧ����ʽ��֪���κε�λʱ��������H2��CO2�����ʵ���֮�Ⱦ�Ϊ3:1����d������������
��������������Ӧѡab��
(3)�������Ϣ�ɷֱ�д���������Ҵ�ȼ���ȱ�ʾ���Ȼ�ѧ����ʽ��H2(g)+1/2O2(g)=H2O(l)��H=-286kJ/mol��CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l)��H=-1300kJ/mol���Ӷ�������������Ҵ���ȼ���ȵı�ֵΪ286kJ/mol:1300kJ/mol=0.22��
(4)����ͼ��֪��������ΪͶ�ϱȣ�������ΪCO2��ת���ʣ�����Ϊ�����ߣ�����ͬͶ�ϱ�ʱ�¶ȵͶ�Ӧ��CO2��ת���ʴ������¶�ƽ��������Ӧ�����ƶ���
����ͼ��֪����700K����ʼͶ�ϱ�n��H2��/n��CO2��=1.5ʱ��������̼ת����Ϊ20%����CO2��H2����ʼ���ʵ����ֱ�Ϊ1mol��1.5mol��ת���Ķ�����̼Ϊ1mol��20%=0.2mol�����ݻ�ѧ����ʽ��֪ת��������Ϊ0.2mol��3=0.6mol��H2��ת����Ϊ0.6mol��1.5mol��100%=40%��
������ʼʱc(CO2)=xmol��L-1������ʼʱc(H2)=2xmol��L-1����
2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)
CH3CH2OH(g)+3H2O(g)
��ʼ(mol/L) x 2x 0 0
ת��(mol/L) 0.6x 1.8x 0.3x 0.9x
ƽ��(mol/L) 0.4x 0.2x 0.3x 0.9x
0.2x=a����x=5a��ƽ��ʱc(CH3CH2OH)=0.3xmol��L-1=1.5amol��L-1��


 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼ�м׳ص��ܷ�ӦʽΪN2H4��O2===N2��2H2O���׳��и����ϵĵ缫��ӦʽΪ_________���ҳ���ʯī�缫�Ϸ����ķ�ӦΪ_______________���׳���ÿ����0.1 mol N2H4���ҳص缫���������_________ g���塣

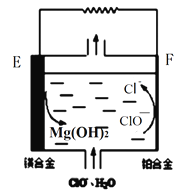
��2��þȼ�ϵ���ڿ��ƶ������豸��Դ�ͱ��õ�Դ�ȷ���Ӧ��ǰ����������ͼΪ��þ������������ȼ�ϵ��ԭ��ʾ��ͼ���缫Ϊþ�Ͻ�Ͳ��Ͻ�EΪ��ȼ�ϵ�ص�_______������������������������F�缫�ϵĵ缫��ӦʽΪ______________��
��3����ͼΪ�绯ѧ����������Ĺ���ʾ��ͼ������Թ������������������ʣ��õ�����ܴ���O2-���ӡ�S(g)�ڸ�������SO3�ĵ缫��ӦʽΪ____________________����֪S(g)�ڸ��������ķ�ӦΪ���淴Ӧ��Ϊ�����������ת���ʣ��ù��ղ�ȡ�Ĵ�ʩ��____________����дһ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����װ�[��CH3��2NH��H2O]��һԪ�������볣��Kb=1.6��10��4��10 mL c mol��L��1���װ���Һ�еμ�0.1mo1��L��1���ᣬ�����Һ���¶�����������Ĺ�ϵ��ͼ��ʾ������˵������ȷ��

A. ���װ���Һ��Ũ��Ϊ0.2mol��L��1
B. ��Y��Z��֮��ij����ҺpH=7
C. Y����ڣ�c��Cl����>c[��CH3��2NH2+]>c��H+��>c��OH����
D. �����£���CH3��2NH2Clˮ�ⳣ��Kh��5.0��10��11
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���һ���ܱ������н������·�Ӧ��NO(g)��CO(g) ![]()
![]() N2(g)��CO2(g)����H����373.2 kJ��mol��1���ﵽƽ���Ϊ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ����ȷ��ʩ��
N2(g)��CO2(g)����H����373.2 kJ��mol��1���ﵽƽ���Ϊ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ����ȷ��ʩ��
A. �Ӵ���ͬʱ�����¶� B. �Ӵ���ͬʱ����ѹǿ
C. �����¶�ͬʱ����N2 D. �����¶�ͬʱ����ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ij�¶�ʱ���� 2 L ������ X��Y��Z �������ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ�����ݷ������÷�Ӧ�Ļ�ѧ����ʽΪ________

(2)������Ϊ��Դȼ�շų��������ȣ���֪��2CH4(g)+3O2(g)=2CO(g)+4H2O(l)��H1��-1214kJ/mol����2CO(g)��O2(g)��2CO2(g) ��H2����566 kJ/mol���ʾ����ȼ�յ��Ȼ�ѧ����ʽΪ__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a mol H2��b mol C2H2���ܱ������з�Ӧ������ﵽƽ��ʱ������c mol C2H4����ƽ����������ȫȼ������CO2��H2O���������������ʵ���Ϊ
A. (![]() )mol B. (a��3b)mol
)mol B. (a��3b)mol
C. (![]() )mol D. (a��3b��2c)mol
)mol D. (a��3b��2c)mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��Ba(OH)2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯����������ͼ��ʾ�����з�������ȷ���ǣ� ��

A. �ٴ����μ�H2SO4��Һ�ı仯����
B. b�㣬��Һ�д������ڵ�������Na+��OH�C
C. c�㣬����Һ�к�����ͬ����OH�C
D. a��d�����Ӧ����Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ������������ˮ�����Һ�����������
B. Ũ����������������ۻ������κ�����¶�����Ӧ
C. ϡ�����ͭ��Ӧ��Ҫ����
D. ̼泥�ָ����̼����泥������ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��֪�� C(s)+O2(g)=CO2(g) ��H1����393.5 kJ/mol
C(s)+H2O(g)=CO(g)+H2(g) ��H2����131.3 kJ/mol
��ӦCO(g)+H2(g) +O2(g)= H2O(g)+CO2(g)����H= _____________kJ/mol��
(2)��һ���ݵ��ܱ�����������CO��H2�ϳɼ״���CO(g)+2H2(g)![]() CH3OH(g) ��H
CH3OH(g) ��H
��������������˵���÷�Ӧ�Ѵﵽƽ��״̬����_________(�����)��
A��ÿ����1 mol CO��ͬʱ����2molH2
B��������������ʵ�������
C������CH3OH������������CO���������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��CO��ƽ��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��A��B�����ƽ�ⳣ��K(A)_______K(B)(������������=����������,��ͬ)����ͼ�ж���H ______0��

��ij�¶��£���2.0 mol CO��6.0 molH2����2 L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c(CO)=0.25 mol/L����CO��ת����=________�����¶��µ�ƽ�ⳣ��K=_________(������λ��Ч����)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com