
【题目】下列叙述正确的是( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42﹣)>c(NH4+)
B.两种醋酸溶液的物质的量浓度分别为c1和c2 , pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3醋酸溶液等体积混合,滴入石蕊试液呈红色
D.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中 ![]() 增大
增大
【答案】C
【解析】解:A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,溶液中氢离子浓度等于氢氧根离子浓度;溶液呈电中性,所以阴阳离子所带电量相等,所以2c(SO42﹣)=c(NH4+),故A错误;B、醋酸是弱电解质,在水溶液中只有部分电离,所以醋酸的浓度大于氢离子浓度;两种醋酸溶液的物质的量浓度分别为c1和c2 , pH分别为a和a+1的两种醋酸溶液中氢离子浓度之比=10:1,当两种酸的电离度相同时,则c1=10c2 , 实际上,两种酸的浓度不等,且浓度越大,酸的电离度越小,所以两种酸的浓度关系为c1>10c2 , 故B错误;
C、pH=11的NaOH溶液的C(NaOH)=10﹣3 mol/L,pH=3醋酸溶液的c(CH3COOH)>10﹣3 mol/L,等体积的两种溶液n(CH3COOH)>n(NaOH),醋酸有剩余,但CH3COOH大于CH3COO﹣水解程度,则等体积混合后溶液呈酸性,所以向混合液中滴入石蕊试液呈红色,故C正确;
D、氨水的电离方程式为:NH3 . H2ONH4++OH﹣ , 当向氨水中加入硫酸铵时,硫酸铵中含有铵根离子,导致氨水的电离平衡向逆反应方向移动,溶液中氢氧根离子浓度降低,氨水的浓度增大,则溶液中 ![]() 减小,故D错误;
减小,故D错误;
故选C.
A、根据溶液呈电中性,即溶液中阴阳离子所带电量相等判断硫酸根离子和铵根离子的关系;
B、醋酸的浓度与醋酸溶液中的氢离子浓度不等;
C、醋酸是弱电解质,醋酸的浓度远远大于氢离子浓度,根据酸碱混合后溶液的酸碱性判断石蕊试液的颜色;
D、根据硫酸铵对氨水电离平衡的影响分析判断.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】环扁桃酸酯的结构简式如图所示,下列说法中不正确的是( )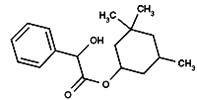
A.环扁桃酸酯的分子式为C17H24O3
B.环扁桃酸酯在水中几乎不溶,在乙醇或丙酮中易溶解
C.环扁桃酸酯可以发生加成、取代、消去等反应
D.1 mol环扁桃酸酯最多可以与1 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填空.
(1)如图1是常见仪器的部分结构. 
①写出仪器名称BC
②使用前需检查是否漏水的仪器有 .
依据表数据列式计算该NaOH溶液的物质的量浓度(保留两位有效数字)
(2)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 . 滴定终点时,锥形瓶中颜色变化为 , 且半分钟内颜色不复原.
依据表数据列式计算该NaOH溶液的物质的量浓度(保留两位有效数字)
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
依据表数据列式计算该NaOH溶液的物质的量浓度 . (保留两位有效数字)
(4)若滴定开始和结束时,酸式滴定管中的液面如图2所示,所用盐酸溶液的体积为mL.
依据表数据列式计算该NaOH溶液的物质的量浓度 . (保留两位有效数字)
(5)某学生根据3次实验分别记录有关数据如表:
滴定 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 25.11 | 25.11 |
第二次 | 25.00 | 0.56 | 30.56 | 30.00 |
第三次 | 25.00 | 0.22 | 25.11 | 24.89 |
依据表数据列式计算该NaOH溶液的物质的量浓度 . (保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A. 酸性氧化物:CO2、SO2、CO
B. 碱:烧碱、纯碱、苛性钾、氢氧化钡
C. 混合物:盐酸、冰水混合物
D. 碱性氧化物:Na2O、CaO、MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在指定溶液中,大量共存的是( )
A.含大量SO2的溶液中:NH4+、F﹣、HCO3﹣、ClO﹣
B.能使淀粉碘化钾试纸变蓝的溶液:Cl﹣、Na+、S2﹣、NH4+
C.![]() =10﹣13mol/L的溶液中:Al3+、Fe3+、NO3﹣、ClO4﹣
=10﹣13mol/L的溶液中:Al3+、Fe3+、NO3﹣、ClO4﹣
D.滴入KSCN溶液显红色的溶液中:NO3+、Na+、AlO2﹣、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化碘(ICl)的化学性质与氯气相似,预计它与NaOH溶液反应的最初生成物可能是
A. NaCl和NaIO B. NaClO和NaI C. NaCl和NaI D. NaClO和NaIO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.
(1)用CH4催化还原煤燃烧产生的氮氧化物,可以消除污染.
已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=﹣867.0kJ/mol
NO2(g)═ ![]() N2O4(g)△H=﹣28.5kJ/mol
N2O4(g)△H=﹣28.5kJ/mol
写出CH4催化还原N2O4(g)生成CO2、N2和H2O(g)的热化学方程式 .
(2)一定条件下,将NO2与SO2以体积比1:2置于恒温恒容的密闭容器中,发生NO2(g)+SO2(g)═SO3(g)+NO(g),测得反应达到平衡时NO2与SO2体积比为1:5,则平衡常数K=(填数值).
(3)如图1是一种用NH3、O2脱除烟气中NO的原理,该原理中NO最终转化为H2O和(填化学式),当消耗1mol NH3和0.5molO2时,除去的NO在标准状况下的体积为L. 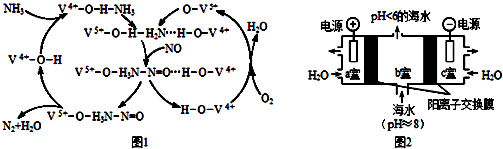
(4)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域.有人利用图2所示装置(均为惰性电极)从海水中提取CO2(海水中无机碳95% 以HCO3﹣存在),有利于减少环境中温室气体含量.
①a室的电极反应式为 .
②b室中提取CO2的反应的离子方程式为 .
③b室排出的海水(pH<6)不可直接排回大海,需用该装置中产生的物质对b室排出的海水进行处理,合格后才能排回大海.处理的方法是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com