
NH3+H2O![]() NH3·H2O
NH3·H2O![]()
![]() +OH-;ΔH>0
+OH-;ΔH>0
在下列情况下,NH3、![]() 、OH-的浓度如何变化?
、OH-的浓度如何变化?
(1)加入NH4Cl晶体:c(OH-)___________,?c(![]() )___________。
)___________。
(2)加入HCl:c(NH3) ___________,?c(OH-)___________。
(3)加入少量NaOH晶体:c(NH3) ___________,c(![]() )___________。
)___________。
科目:高中化学 来源: 题型:
| 加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c(OH-)的变化 | ① 减小 减小 |
② 减小 减小 |
③ 增大 增大 |
| 平衡移动方向 | ④ 左移 左移 |
⑤ 右移 右移 |
⑥ 左移 左移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
+ 4 |
+ 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
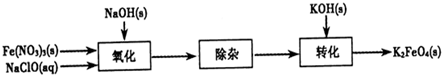
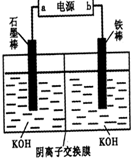
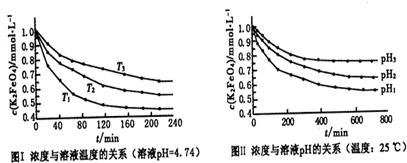
查看答案和解析>>
科目:高中化学 来源: 题型:
在稀氨水中存在电离平衡NH3·H2O![]() NH4+ + OH-,如果进行下列操作,用“增大”、“减小”、“不变”填空:
NH4+ + OH-,如果进行下列操作,用“增大”、“减小”、“不变”填空:
(1)通入适量HCl气体时,c(NH4+) ________,c(H+) ______________
(2)加入少量NaOH固体,c(NH4+) ____,c(OH-) ________
(3)加入NH4Cl晶体时,c(NH4+) __ ,c(OH-) ______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com