
| A. | 在周期表中处于第3周期 VIIA | B. | 在周期表中处于第2周期VA族 | ||
| C. | 氢化物比PH3稳定 | D. | 常见化合价有-3、+2、+3、+5价 |
科目:高中化学 来源: 题型:解答题
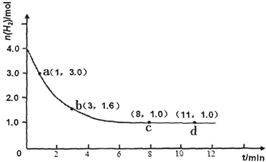
 在MgCl2和AlCl3的混合液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示.
在MgCl2和AlCl3的混合液中,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
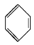 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ 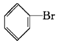 +HBr.
+HBr.| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
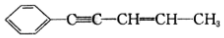 ,有关其结构说法正确的是( )
,有关其结构说法正确的是( )| A. | 同一平面上的碳原子至少有9个 | B. | 所有碳原子可能在同一条直线上 | ||
| C. | 所有碳原子不可能在同一平面上 | D. | 所有碳原子可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W与氢形成的原子比为1:1的化合物有多种 | |
| B. | X的氢化物只含有极性共价键 | |
| C. | Y单质可通过电解Y的氯化物获得 | |
| D. | W与Z形成化合物WZ2中各原子均满足8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | C | C. | Mg | D. | Na |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com