
利用下列实验装置能完成相应实验的是 ( )

C.装置③制备纯净的NH3 D.装置④比较MnO2、Cl2、S的氧化性
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为( )
A.2∶1∶2 B.2∶1∶3
C.6∶3∶2 D.3∶7∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为CnH2nO2的羧酸和某醇酯化生成分子式为Cn+2H2n+4O2的酯,参加反应的羧酸和醇的质量比为1∶1,则该羧酸是
A.乙酸 B.丙酸 C.甲酸 D.乙二酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①离子化合物含离子键,也可能含极性键或非极性键 ②H2SO3的酸性>H2CO3的酸性,所以非金属性S>C ③含金属元素的化合物不一定是离子化合物 ④由非金属元素组成的化合物一定是共价化合物 ⑤熔融状态能导电的化合物是离子化合物 ⑥由分子组成的物质中一定存在共价键
A.①③⑤⑥ B.②④⑥ C.①②③⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
本题共2个小题,请按要求作答。
(1)(10分)根据下列各组物质,回答问题(均填选项号):
A.O2与O3 B. 12C与13C C .正丁烷和异丁烷
.正丁烷和异丁烷
 |
 E
E .甲烷和庚烷 F.D与T
.甲烷和庚烷 F.D与T
G.金刚石与“足球烯”C60 H.16O、17O和18O
①互为同位素的是 ; ②互为同素异形体的是 ;
③属于同系物的是  ; ④互为同分异构体的是 ;
; ④互为同分异构体的是 ;
⑤属于同一物质的是 。
(2)(5分)用Cl2生产某些含氯有机物时会产生副产物HCl。利用下列反应,可实现氯的循环利用。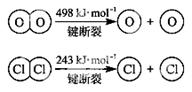
反应:4HCl+O2 = 2Cl2+2H2O
已知:该反应中, 4mol HCl被氧化,放出115.6 kJ的热量。
①H2O的电子式为__________。
②该反应中反应物的总能量_____________ 生成物的总能量。(填“大于、小于或等于”)
③断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为________kJ,H2O中H—O键比HCl中H—Cl键________(填“强”或“弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42-
B.常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中c(OH-)/c(H+)=1012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:
c(B+)>c(OH-)>c(A-)>c(H+)
C.将等浓度的K2S和KHSO4两种溶液等体积,则混合溶液中离子浓度的大小关系为:c(K+)>c(SO42-)>c(HS-)>c(OH-)>c(H+)>c(S2-)
D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍
(已知:Ksp(Cd(OH)2)=7.2×10-15,Ksp(Co(OH)2)=1.8×10-15)
查看答案和解析>>
科目:高中化学 来源: 题型:
将64 g铜箔加入到盛有含2 mol H2SO4的浓H2SO4试管中加热。
(1)铜箔能否完全溶解?请解释原因。
(2)在反应后的溶液中再加入少量硝酸钠晶体,铜箔表面又有气泡冒出,其原因为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
寒冷的冬天,经常使用暖宝宝,暖宝宝中装的是铁粉、活性炭、无机盐等物质,打开包装以后,可以连续12个小时释放热量,以下分析错误的是
A.将化学能转化为热能
B.其发热原理与钢铁的吸氧腐蚀相同
C.铁作负极,电极反应为:Fe – 3e → Fe3+
D.活性炭作正极,电极反应为:2H2O + O2 + 4e → 4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com