
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为_________;
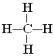
(2)②的气态氢化物分子的结构式为___________,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____(填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________(填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________(填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____。
【答案】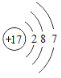
 SiH4 HNO3>H2CO3 减小 减小
SiH4 HNO3>H2CO3 减小 减小 ![]()
【解析】
(1)根据元素在周期表中的位置可知⑧为Cl,Cl的原子结构示意图为: ,故答案为:
,故答案为: ;
;
(2)②是C元素,其简单氢化物为CH4,其结构式为 ,⑦是Si元素,②⑦位于同主族,同主族从上往下非金属性减弱,气态氢化物的稳定性减弱,即气态氢化物稳定性较弱的是SiH4,故答案为:
,⑦是Si元素,②⑦位于同主族,同主族从上往下非金属性减弱,气态氢化物的稳定性减弱,即气态氢化物稳定性较弱的是SiH4,故答案为: ;SiH4;
;SiH4;
(3)②、③是同周期的元素,同周期从左往右,非金属性增强,其最高价氧化物对应的水化物的酸性就越强,所以最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3,故答案为:HNO3>H2CO3;
(4)⑤、⑥元素是同周期的元素,同周期从左往右,金属性减弱,所以⑤、⑥元素的金属性强弱依次减小,故答案为:减小;
(5)④、⑤、⑥三种元素形成的简单离子电子层结构相同,元素的原子序数越大,离子半径就越小,即④、⑤、⑥离子半径依次减小,故答案为:减小;
(6)①、④、⑤元素分别是H、O、Na,它们可形成既含离子键又含共价键的化合物NaOH,它的电子式是:![]() ,故答案为:
,故答案为:![]() 。
。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】已知:2SO2(g)+O2(g)=2SO3(g) △H,有关数据如下:

下列说法不正确的是( )
A.根据平衡常数随温度的变化关系,判断出△H<0
B.保持其他条件不变,SO2的平衡转化率a(727℃)<a(927℃)
C.增大压强、降低温度能提高SO2的转化率
D.SO3的稳定性随温度的升高而降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在用氨气饱和的食盐水中通入足量二氧化碳可生成NaHCO3固体,反应原理如下: NH3+CO2+H2O=NH4HCO3 NH4HCO3+NaCl=NaHCO3↓+NH4Cl,化学兴趣小组同学根据该原理和如下装置在实验室制备NaHCO3。

实验步骤如下:
Ⅰ、连接好如图装置,检查气密性后,在仪器内装入相应药品。
Ⅱ、在丙装置制备氨气,并通入到丁中饱和食盐水中,直至不再溶解时,然后在饱和食盐水中通入二氧化碳气体,片刻后,丁装置广口瓶中出现固体。继续向广口瓶中通入两种气体,直到不再有固体产生。
Ⅲ、过滤丁中广口瓶中所得的混合物,洗涤、干燥,得到NaHCO3固体。
(1)盛装盐酸的仪器名称是_____________。
(2)乙中溶液是_______(填字母代号)。
A.浓硫酸 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(3)装置的部分连接顺序是:a接________(填“c”或“d”);丁装置中球形干燥管的作用是_________________________________。
(4)请解释在实验步骤Ⅱ中,先通入氨气的理由是________________________________________。
(5)取m g NaHCO3样品(杂质只含有少量NaCl)溶于足量盐酸,蒸干后称得固体质量为n g,则样品中NaHCO3的质量分数为_____________(用含m、n的代数式表示,不用化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用原电池原理,在室温下从含低浓度铜的酸性废水中回收铜的实验装置如图所示,下列说法错误的是

A. X、Y依次为阳离子、阴离子选择性交换膜
B. 负极的电极反应式:BH4-+8OH-一8e-═B(OH)4-+4H2O
C. 2室流出的溶液中溶质为Na2SO4和K2SO4
D. 电路中每转移1mol电子,电极2上有32gCu析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量![]() N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
(1)写出该反应的热化学方程式_______________________________________.
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol﹣1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ.
(3)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣a kJ·mol﹣1
途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol﹣1
2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=﹣c kJ·mol﹣1
2H2(g)+O2 (g)═2H2O(l)△H=﹣d kJ·mol﹣1 (abcd均为正值)
请回答下列问题:
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量_______(填“大于”、“等于”或“小于”)途径II放出的热量.
②在C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量________(填“大于”、“等于”或“小于”)生成物具有的总能量.
③b 与a、c、d的数学关系式是_____________.
II、利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol·L1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)为什么所用NaOH溶液要稍过量?__________________________。
(2)假设盐酸和氢氧化钠溶液的密度都是1 g·cm3,又知中和反应后生成溶液的比热容c=4.18 J·g1·℃1。为了计算中和热,某学生实验记录数据如下:
实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠 | ||
1 | 20.0 | 20.0 | 23.0 |
2 | 20.1 | 20.1 | 23.2 |
3 | 20.2 | 20.2 | 23.4 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=________kJ·mol1_(结果保留一位小数)。
(3)不能用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. WZ的水溶液呈碱性
B. 元素非金属性的顺序为X>Y>Z
C. Y的最高价氧化物的水化物是中强酸
D. 该新化合物中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】GaN是制造5G芯片的材料,氮化镓铝和氮化铝LED可发出紫外光。回答下列问题:
(1)基态As原子核外电子排布式为[Ar]___,下列状态的铝中,电离最外层的一个电子所需能量最小的是___(填标号)。
A.![]() B.
B.![]() C.[Ne] D.
C.[Ne] D.![]()
(2)8一羟基喹啉铝(分子式C27H18AlN3O3)用于发光材料及电子传输材料,可由LiAlH4与(8一羟基喹啉 )合成。LiAlH4中阴离子的空间构型为____;所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为____、_____和____。
)合成。LiAlH4中阴离子的空间构型为____;所含元素中电负性最大的是___(填元素符号),C、N、O的杂化方式依次为____、_____和____。
(3)已知下列化合物的熔点:
化合物 | AlF3 | GaF3 | AlCl3 |
熔点/°C | 1040 | 1000 | 194 |
①表中卤化物的熔点产生差异的原因是_____。
②熔融AlCl3时可生成具有挥发性的二聚体Al2Cl6,二聚体Al2Cl6的结构式为____;其中Al的配位数为____。
(4)GaAs的晶胞结构如图所示,其晶胞参数为apm。

①紧邻的As原子之间的距离为x,紧邻的As、Ga原子之间的距离为y,则![]() __。
__。
②设阿伏加德罗常数的值为NA,则GaAs的密度是___g·cm一3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红热的铁能与水蒸气反应,有氢气生成,现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气,请回答下列问题:

(1)写出铁与水蒸气反应的化学方程式:________________________。
(2)干燥管C内盛放的药品是__________或__________。干燥管的__________(填“m”或“n”)端与g导管相连接。
(3)怎样用简单的方法检验收集到的气体是氢气,简述实验操作步骤和现象:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
①在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为__________________________。
②甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
a.CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) △H1=+49.0kJ·mol—1
CO2(g)+3H2(g) △H1=+49.0kJ·mol—1
b. ![]() △H2
△H2
已知H2(g)+ ![]() O2(g)
O2(g) ![]() H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
则反应②的△H2=_________ kJ·mol-1。
(2)工业上一般可采用下列反应来合成甲醇:CO(g)+2H2(g)CH3OH(g),现实验室模拟该反应并进行分析,图1是该反应在不同温度下CO的转化率随时间变化的曲线。
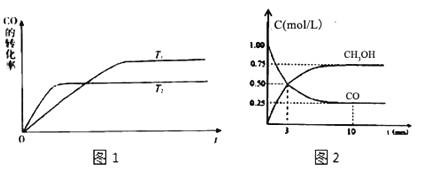
①该反应的焓变△H_____0(填“>”“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1_____K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡,CO的平均反应速率v(CO)=_____,该反应的平衡常数为K=_____。
④恒容条件下,达到平衡后,下列措施中能使![]() 增大的有_____。
增大的有_____。
A.升高温度 B.充入He(g)
C.再充入1molCO 和3molH2 D.使用催化剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com