
【题目】对于反应:![]() (Q>0),达到平衡后,改变一个条件,以下有关分析正确的是
(Q>0),达到平衡后,改变一个条件,以下有关分析正确的是
A.升高温度,正反应速率增大,化学平衡常数增大
B.减小压强,逆反应速率减小,化学平衡常数减小
C.加入催化剂,正逆反应速率不变,平衡不移动
D.充入氧气,正反应速率先增大后减小,平衡向正反应方向移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)写出醋酸的电离方程式:_____________________________________;
(2)写出醋酸电离平衡常数表达式:_______________;
(3)向0.1mol/L 醋酸溶液中加入水,电离平衡向_______移动 (填“左”或“右”) ;n(CH3COOH)_______; c(CH3COO-)/c(H+)_______(填“增大”、“减小”或“不变”);
(4)500mL 0.1mol/L 醋酸溶液a和500mL 0.1mol/L 盐酸溶液b与足量Zn粉反应,初始速率a___b;生成H2的量a____b;完全中和这两种酸,消耗NaOH的量a___b(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇结构式为 ,“箭头”表示乙醇发生化学反应时分子中可能断键的位置,下列叙述中不正确的是
,“箭头”表示乙醇发生化学反应时分子中可能断键的位置,下列叙述中不正确的是
A. 与钠反应时断裂①键 B. 发生消去反应时断裂②④键
C. 发生催化脱氢反应时断裂①③键 D. 与乙酸发生酯化反应时断裂②键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指出下列化学反应类型(氧化、酯化、加成、取代)
(1)CH2Cl2+Br2![]() CHBrCl2+HBr _____________
CHBrCl2+HBr _____________
(2)CH2=CH2+Br2→CH2BrCH2Br __________
(3)![]() +HNO3
+HNO3![]()
![]() NO2 +H2O _______________
NO2 +H2O _______________
(4)![]() ___________
___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完成下列反应的化学方程式:(注明反应的条件,并配平方程式)
①实验室制乙炔:_________
②向苯酚钠溶液中通入二氧化碳气体:________
③甲苯与氯气在光照条件下反应生成一氯取代产物:___
(2)有机物A的结构简式为
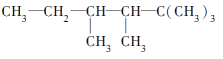
①若A是单烯烃与氢气加成后的产物,则该单烯烃可能有____种结构(不考虑立体异构);
②若A是炔烃与氢气加成后的产物,则此炔烃可能有____种结构;
③若A的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个非常对称的分子构型,有顺、反两种结构。
写出A的该种同分异构体(包括顺反异构)的结构简式______、_____;
(3)C5H12O的同分异构体有____种,其中属于醇类且能被氧化成醛的有____种,能消去H2O生成烯的醇有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA是阿伏加德罗常数的值,下列说法正确的是
A. 0.1mol FeCl3水解形成的Fe(OH)3胶体粒子数为0.1 NA
B. 常温下,78 g Na2O2中含有的阴离子数是2NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. pH=1的H2SO4溶液中,含有H+的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15. 2MPa条件下又重复吸氢。NaAlH4可由AlCl3和NaH在适当条件下合成。NaAlH4的晶胞结构如图所示。
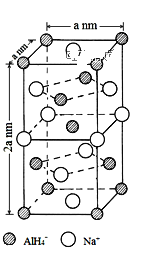
(1)基态Ti原子的价电子轨道排布图为___________。
(2)NaH的熔点为800℃,不溶于有机溶剂。NaH属于_____晶体,其电子式为____________。
(3)AlCl3在178℃时升华,其蒸气的相对分子质量约为267,蒸气分子的结构式为______________ (标明配位键)
(4)AlH4-中,Al的轨道杂化方式为_______;例举与AlH4-空间构型相同的两种离子_________(填化学式)。
(5)NaAlH4晶体中,与Na+紧邻且等距的AlH4-有______个;NaAlH4晶体的密度为______________g·cm-3(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
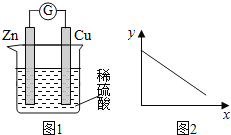
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com