
| A. | 过滤 | B. | 蒸发 | C. | 分液 | D. | 萃取 |
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝溶于氢氧化钠溶液:Al+2OH-+H2O═AlO${\;}_{2}^{-}$+2H2↑ | |
| B. | 铜片投入少量FCl3溶液中:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C. | .Ca(CHO3)2溶液与足量澄清石灰水混合:Ca2++HCO${\;}_{3}^{-}$+OH-═CaCO3↓+H2O | |
| D. | 用铁棒作电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+O2↑+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x与y的关系如图所示.请回答下列问题:
某温度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x与y的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
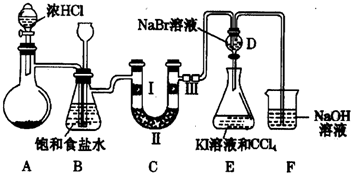
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4分子的球棍模型: | |
| B. | 中子数为146、质子数为92的铀原子${\;}_{92}^{146}$U | |
| C. | 氟化钠的电子式: | |
| D. | 正丁烷的结构简式:C4H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若金属全部溶解,则溶液中一定含有Fe3+ | |
| B. | 若金属有剩余,向溶液中再滴入硫酸后,金属不会发生溶解 | |
| C. | 当溶液中金属离子只含有Fe3+、Cu2+时,则c与a、b的关系为:c=80a$\frac{1-b}{3}$ | |
| D. | 若金属全部溶解,且产生336mL气体(标准状况),则c=0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | m=n | B. | m>n | C. | m<n | D. | m≤n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com