
“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
(4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0) (16分)
(1)①2.67(2分) ②<1 (2分) ③< (2分)
(2)5.6×10—5mo1/L (2分)
(3)+172.5 (2分)
(4)FePO4+Li++e—=LiFePO4(2分) Li-e—=Li+(2分) 1.4 g(2分)
解析试题分析:(1)①表中实验1有关组分的起始物质的量、平衡物质的量已知,容器体积为2L,由于c=n/V,则
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始浓度(mol/L) 2 1 0 0
变化浓度(mol/L) 0.8 0.8 0.8 0.8
平衡浓度(mol/L) 1.2 0.2 0.8 0.8
K=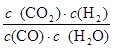 =
=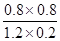 =2.67
=2.67
②实验3中CO、H2O的起始浓度分别为a/2mol/L、b/2mol/L,设CO的变化浓度为xmol/L,由于CO、H2O的变化浓度之比等于化学方程式的系数之比,则H2O的变化浓度为xmol/L,则CO、H2O的平衡转化率分别为2x/a、2x/b,若CO的平衡转化率大于水蒸气,则2x/a>2x/b,所以a/b<1;
③先根据实验2中有关数据求900时的平衡常数,再根据温度不变平衡常数不变,利用此时各组分的物质的量计算各自浓度,根据浓度商与平衡常数的大小判断此时反应进行的方向(若浓度商大于平衡常数,则反应向逆反应方向进行,反之,则向正反应方向进行),最后反应向哪个方向进行,则哪个方向的速率就大于相反方向的速率。
表中实验2有关组分的起始物质的量、平衡物质的量已知,容器体积为2L,由于c=n/V,则
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始浓度(mol/L) 1 0.5 0 0
变化浓度(mol/L) 0.2 0.2 0.2 0.2
平衡浓度(mol/L) 0.8 0.3 0.2 0.2
K=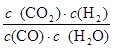 =
=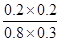 =0.167
=0.167
实验4时CO、H2O、CO2、H2的浓度分别为5mol/L、2.5mol/L、1mol/L、2.5mol/L,则Q=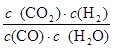 =
=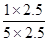 =0.2>K=0.167,说明此时反应应该向逆反应方向进行,所以v(逆)>v(正),即v(正)<v(逆);
=0.2>K=0.167,说明此时反应应该向逆反应方向进行,所以v(逆)>v(正),即v(正)<v(逆);
(2)设混合前CaCl2溶液的最小浓度为xmol/L,Na2CO3溶液的浓度为2×10—4mo1/L,则等体积混合后CaCl2、Na2CO3的浓度分别为x/2mol/L、1×10—4mo1/L,则Ksp=2.8×10—9= x/2×1×10—4,x=5.6×10—5;
(3)先将3个热化学方程式依次编号为①②③,接着观察它们的关系,发现①/2—②/2=③,则C(s) + CO2(g) = 2CO(g)的△H3=△H1 /2—△H2/2="+172.5" kJ/mol;
(4)放电时电池总反应式为FePO4+Li=LiFePO4,其中锂元素由0升为+1价,铁元素由+3降为+2价,前者在负极上发生氧化反应,后者在正极上发生还原反应,根据电子、电荷、原子守恒原理及电解质中定向移动的离子环境,正极反应式为FePO4+Li++e—=LiFePO4,负极反应式为Li-e—=Li+;用惰性电极电解水的原理为2H2O 2H2↑+O2↑~4e—,则n(H2)=2n(O2),由于n=V/Vm,则n(H2)+n(O2)="3" n(O2)=3.36L÷22.4L/mol=0.15mol,则n(O2)=0.05mol,则转移电子的物质的量="4" n(O2)=0.2mol,由于新型电池中转移电子和电解水时转移电子相等,FePO4+Li=LiFePO4~e—中参加反应的锂与转移电子的系数之比等于物质的量之比,则参加反应的锂为为0.2mol,由于锂的相对原子质量约为7.0,m=n×M,则参加反应的锂为1.4g。
2H2↑+O2↑~4e—,则n(H2)=2n(O2),由于n=V/Vm,则n(H2)+n(O2)="3" n(O2)=3.36L÷22.4L/mol=0.15mol,则n(O2)=0.05mol,则转移电子的物质的量="4" n(O2)=0.2mol,由于新型电池中转移电子和电解水时转移电子相等,FePO4+Li=LiFePO4~e—中参加反应的锂与转移电子的系数之比等于物质的量之比,则参加反应的锂为为0.2mol,由于锂的相对原子质量约为7.0,m=n×M,则参加反应的锂为1.4g。
考点:考查化学反应原理,涉及求化学平衡常数、比较反应物的平衡转化率、浓度商与平衡常数大小关系、反应进行方向与正、逆反应速率大小的关系、稀释定律、溶度积计算、盖斯定律、原电池和电解原理、电极反应式、物质的量、气体摩尔体积、摩尔质量、物质的量在化学或离子方程式计算中的应用等。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:问答题
(15分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4= K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |

| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05 mol/L KMnO4溶液 | |||
| 4 | 3.0 | 2.0 | 2.0 | 3.0 | | t |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
以白云石(化学式表示为MgCO3·CaCO3)为原料制备Mg(OH)2的工艺流程如下图所示。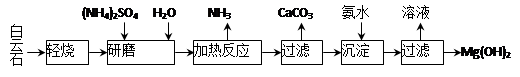
(1)研磨的作用是 。
(2)该工艺中可循环使用的物质是 、 (写化学式)。
(3)白云石轻烧的主要产物是MgO·CaCO3,而传统工艺是将白云石加热分解为MgO和CaO后提取,白云石轻烧的优点是 。
(4)加热反应的离子方程式为 。
(5)①加热反应时,在323k和353k溶液中c(NH4+)与反应时间的关系如下图所示,请在下图画出373k的曲线。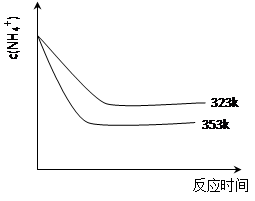
②由图可知,随着温度升高: 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
消除汽车尾气是减少城市空气污染的热点研究课题。
(1)汽车内燃机工作时发生的反应N2(g) + O2(g) 2NO(g),生成的NO是汽车尾气的主要污染物。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol(不考虑后续反应)。则:
2NO(g),生成的NO是汽车尾气的主要污染物。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol(不考虑后续反应)。则:
①5 min内该反应的平均速率ν(NO) = ;在T ℃时,该反应的平衡常数K = 。
② 反应开始至达到平衡的过程中,容器中下列各项发生变化的是 (填序号)。
a.混合气体的密度 b.混合气体的压强
c.正反应速率 d.单位时间内,N2和NO的消耗量之比
(2)用H2或CO催化还原NO可以达到消除污染的目的。
已知:2NO(g) = N2(g) + O2(g) ? △H =" —180.5" kJ·mol-1
2H2O(l) =2H2(g) + O2(g) ?△H =" +571.6" kJ·mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是
。
(3)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应2NO(g) + 2CO(g)
 2CO2(g) + N2(g) 中,NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2(g) + N2(g) 中,NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
① 该反应的?H 0 (填“>”或“<”)。
②若催化剂的表面积S1>S2 ,在右图中画出c(NO) 在T1、 S2 条件下达到平衡过程中的变化曲线(并作相应标注)。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)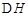 =-49.0kJ·mol
=-49.0kJ·mol
某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。回答下列问题: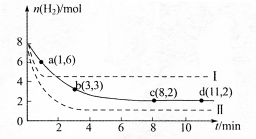
(1)该反应在0~8min内CO2的平均反应速率是 mol·L-1·min-1
(2)此温度下该反应的平衡常数K的数值为 。
(3)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。
与实线相比,曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是 。若实线对应条件下平衡常数为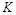 ,曲线Ⅰ对应条件下平衡常数为
,曲线Ⅰ对应条件下平衡常数为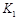 ,曲线Ⅱ对应条件下平衡常数为
,曲线Ⅱ对应条件下平衡常数为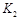 ,则
,则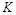 、
、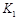 和
和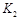 的大小关系是 。
的大小关系是 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
2012年2月27日深圳宣称进入“200万辆汽车时代”,汽车尾气已成为重要的空气污染物。
(1)汽车内燃机工作时引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向2L密闭容器中充入4mol N2和6molO2,5min后达平衡时NO物质的量为4mol,该反应的速率v(N 2)为 ;计算该条件下的平衡常数(写出计算过程)。
2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向2L密闭容器中充入4mol N2和6molO2,5min后达平衡时NO物质的量为4mol,该反应的速率v(N 2)为 ;计算该条件下的平衡常数(写出计算过程)。
(2)恒温恒容,能说明反应 2NO(g)  N2(g)+O2(g) 达到平衡的是 (填代号)。
N2(g)+O2(g) 达到平衡的是 (填代号)。
| A.NO、N2、O2的浓度之比为2∶1∶1 |
| B.N2的浓度不再发生变化 |
| C.单位时间内消耗2 mol NO,同时消耗1 mol N2 |
| D.容器内气体密度不再发生变化 |
 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,据此判断该反应的△H 0 (填“>”、“<”或“无法确定”)。若催化剂的表面积S1>S2 ,在下图中画出NO的浓度在T1、S2条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,据此判断该反应的△H 0 (填“>”、“<”或“无法确定”)。若催化剂的表面积S1>S2 ,在下图中画出NO的浓度在T1、S2条件下达到平衡过程中的变化曲线,并注明条件。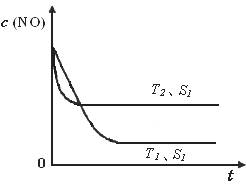
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(16分)Na2S2O8溶液可降解有机污染物4-CP,原因是Na2S2O8溶液在一定条件下可产生强氧化性自由基(SO4-)。通过测定4-CP降解率可判断Na2S2O8溶液产生(SO4-·)的量。某研究小组探究溶液酸碱性、Fe2+的浓度对产生(SO4-·)的影响。
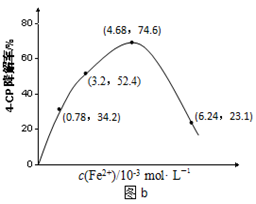
(1)溶液酸碱性的影响:其他条件相同,将4-CP加入到不同pH的Na2S2O8溶液中,结果如图a所示。由此可知:溶液酸性增强, (填 “有利于”或“不利于”)Na2S2O8产生SO4-·。
(2)Fe2+浓度的影响:相同条件下,将不同浓度的FeSO4溶液分别加入c(4-CP)=1.56×10-4 mol·L-1、c(Na2S2O8)=3.12×10-3 mol·L-1的混合溶液中。反应240 min后测得实验结果如图b所示。
已知 S2O82- + Fe2+= SO4-·+ SO42- + Fe3+,此外还可能会发生:SO4-· + Fe2+=SO42- + Fe3+
① 实验开始前,检验FeSO4溶液是否被氧化的试剂是 (化学式)。如被氧化可以观察到的现象是 。
②当c(Fe2+)=3.2 ×10-3 mol·L-1时,4-CP降解率为 %,4-CP降解的平均反应速率的计算表达式为 。
③当c(Fe2+)过大时,4-CP降解率反而下降,原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图1、2所示的实验。请回答相关问题。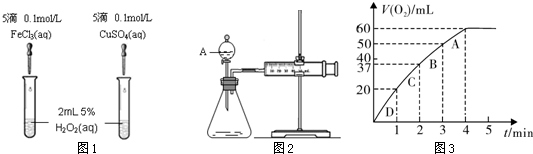
(1)定性分析:如图1可通过观察 ,定性比较得出结论。有同学提出将FeCl3改为0.05 mol/L Fe2(SO4)3更为合理,其理由是 。
(2)定量分析:如图2所示,实验时均生成40 mL气体,其它可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示。
①写出H2O2在二氧化锰作用下发生反应的化学方程式 。
②实验时放出气体的总体积是 mL。
③A、B、C、D各点反应速率快慢的顺序为: > > > 。
解释反应速率变化的原因 。
④H2O2的初始物质的量浓度是 (请保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,将amol·L-1的氨水与bmol·L-1盐酸等体积混合,已知相同条件下氨水的电离程度大于NH4+的水解程度,则下列有关推论不正确的是
| A.若混合后溶液pH=7,则c(NH4+)=c(Cl-) |
| B.若b=2a,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.若a=2b,则c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D.若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com