
【题目】下列离子方程式正确的是( )
A. 漂白粉露置在空气中失效:ClO-+CO2+H2O===HClO+HCO3-
B. 向银氨溶液中加入足量的HCl:[Ag(NH3)2]++OH-+3H+===Ag++2NH4++H2O
C. 过量的CO2通入水玻璃中:SiO32-+2CO2+2H2O===H2SiO3↓+2HCO3-
D. NH4Al(SO4)2溶液中加入过量Ba(OH)2溶液:NH4++Al3++5OH-===NH3·H2O+AlO2-+2H2O
【答案】C
【解析】
A,漂白粉露置在空气中失效的反应为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO、2HClO![]() 2HCl+O2↑,CaCO3难溶于水以化学式保留,漏写HClO的分解反应,A项错误;B,Ag+与Cl-形成AgCl沉淀,正确离子方程式为[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O,B项错误;C,过量CO2与Na2SiO3溶液反应生成NaHCO3和H2SiO3,C项正确;D,漏写Ba2+与SO42-形成BaSO4沉淀,正确的离子方程式为NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3·H2O+AlO2-+2H2O,D项错误;答案选C。
2HCl+O2↑,CaCO3难溶于水以化学式保留,漏写HClO的分解反应,A项错误;B,Ag+与Cl-形成AgCl沉淀,正确离子方程式为[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O,B项错误;C,过量CO2与Na2SiO3溶液反应生成NaHCO3和H2SiO3,C项正确;D,漏写Ba2+与SO42-形成BaSO4沉淀,正确的离子方程式为NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3·H2O+AlO2-+2H2O,D项错误;答案选C。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:高中化学 来源: 题型:
【题目】以H2+Cl2=2HCl为例分析反应过程中能量的变化:
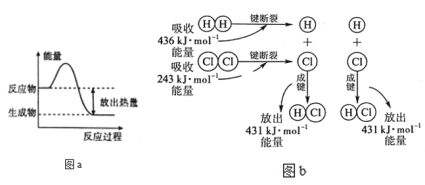
(1)由图a可知:反应物所具有的总能量__生成物所具有的总能量(填“大于、小于或等于”),所以该反应要___(吸收或放出)能量,能量变化值的大小△E=____(用E反和E生表示)。
(2)由图b可知:断裂反应物中的化学键吸收的总能量为E吸=___kJ;形成生成物中的化学键放出的总能量为E放=_____kJ。所以该反应要____(填“吸收” 或“放出”)____kJ(填数值)的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A. 该反应的化学方程式为6A+2 D![]() 3B+4C
3B+4C
B. 反应进行到1 s时,v(A)=v(B)
C. 反应进行到5 s时,B的平均反应速率为0.06mol/(L·s)
D. 反应进行到5 s时,v(A)=v(B)=v(C)=v(D)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是( )
A. 甲酸与乙二酸互为同系物
B. 乙烯和乙烷可用溴的四氯化碳溶液鉴别
C. 分子式为C4H10O且可与金属钠反应放出氢气的有机化合物有6种
D. 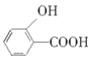 (水杨酸)与足量的NaHCO3溶液反应可生成
(水杨酸)与足量的NaHCO3溶液反应可生成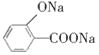 、CO2和H2O
、CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列叙述错误的是
①18 g金刚石中,碳碳共价键数为3NA
②1mol铜与足量硫蒸气反应,转移电子数为 NA
③常温常压时S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
④一定温度下,1 L 0.50 mol·L━1NH4Cl溶液与2 L 0.25mol·L━1NH4Cl溶液中NH4+的物质的量均小于0.5NA,且前者更少
⑤电解法精炼铜时,当阳极质量减少64g时,电路中通过的电子数一定为2NA
A. ② B. ②④⑤ C. ④⑤ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取肥皂的实验有以下步骤:
①在一个干燥的蒸发皿中加入植物油8mL、乙醇8mL、NaOH溶液4mL
②在不断搅拌下,给蒸发皿中液体微微加热,直到混合物变稠
③继续加热,直到皂化反应完成
④把盛混合物的蒸发皿放在冷水浴中冷却.等待片刻,向混合物中加20mL热蒸馏水,再放在冷水中冷却.然后加入25mL NaCl饱和溶液充分搅拌
⑤用纱布滤出固体物质,弃去滤液.把固体物质挤于、压成条状、晾干,即得肥皂
根据实验,填空:
(1)在制肥皂时加入乙醇是利用了乙醇的什么性质?_________;
(2)如何验证皂化反应已完成?_________;
(3)在操作④中加入饱和NaCl溶液的作用是_________;
(4)写出硬脂酸甘油酯发生皂化反应的化学方程式_________;
(5)取用蒸发皿用的仪器是_________;
(6)工业上大规模生产用水蒸气加热的优点_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是

A. Ⅰ、Ⅱ装置之间缺少干燥装置
B. Ⅲ装置后缺少干燥装置
C. Ⅱ 装置中玻璃管内有水冷凝
D. CuO没有全部被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Cl溶于重水(D2O)后,溶液中存在的一水合氨和水合氢离子可能是( )
A.NH3HDO和D3O+B.NH3HDO和HD2O+C.NH3H2O和H2DO+D.以上都有可能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com