
| A. | 只有②③ | B. | 只有② | C. | 只有②③④ | D. | 全部正确 |
分析 ①固体药品的取用要用镊子或药匙;
②用灯帽盖灭酒精灯,不可用嘴吹;
③试管中液体的体积不得超过容积的三分之二;
④用于萃取实验的萃取剂和溶剂互不相溶;
⑤量筒不能作为稀释仪器;
⑥容量瓶不能存放热溶液.
解答 解:①固体氯化钠药品的取用要用药匙或纸槽,故①错误;
②要用灯帽盖灭酒精灯,不可用嘴吹,防止导致内部酒精燃烧爆炸,故②正确;
③试管中液体的体积不得超过容积的三分之二,不能少于四分之一,所以30mL试管中盛放液体要小于20mL,大于7.5mL,故③错误;
④酒精、水以及碘是互溶的,不会发生萃取现象,应该用四氯化碳或苯作萃取剂,故④错误;
⑤量筒不能作为稀释仪器,只能量取一定体积的液体,应该在烧杯中稀释浓硫酸,故⑤错误;
⑥容量瓶不能倒入超过使用温度的热溶液,可待液体冷却后再注入容量瓶中,故⑥错误.
故选B.
点评 本题考查化学实验基本操作,为高频考点,明确化学实验操作原理及操作规范性是解本题关键,注意仪器的选取和使用方法,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

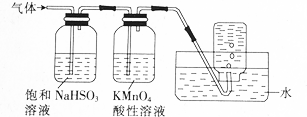
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3固体 | B. | 水 | C. | 硫酸钾固体 | D. | NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水属于化合物 | |
| B. | 一水合氨属于电解质 | |
| C. | 氨气溶于水时,只有极少数氨气与水结合生成一水合氨 | |
| D. | 氨气能使湿润的蓝色石蕊试纸变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
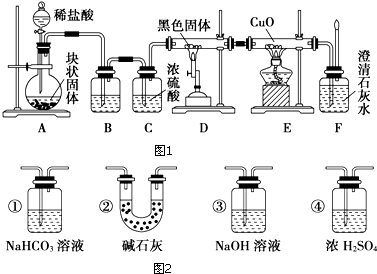
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
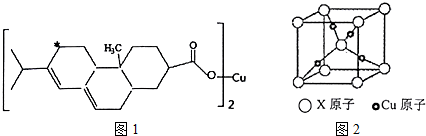
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
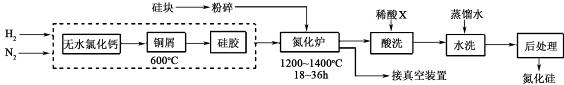
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com