
【题目】将等物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是 ( )
A. CH3ClB. CH2Cl2C. CCl4D. HCl
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )
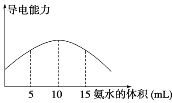
A. 0.5% B. 1.0% C. 0.1% D. 1.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃(聚甲基丙烯酸甲酯)具有透光率高、自重轻、安全性能高等优点,目前它广泛用于制作仪器仪表零件、照明灯罩、光学镜片、透明屋顶、电话亭、广告灯箱、标志牌等。
下图是以2—甲基丙烯为原料合成有机玻璃E(聚—2—甲基丙烯酸甲酯)的路线:
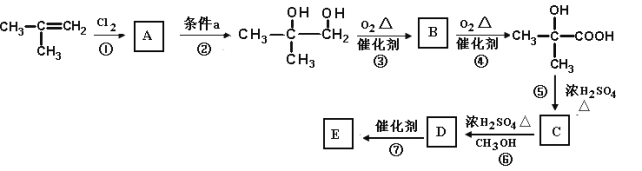
(1)有机化合物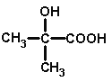 中含有的官能团名称是_____________________________________。
中含有的官能团名称是_____________________________________。
(2)写出B的结构简式:___________________________________
(3)写出反应①的化学方程式____________________________________________________________________
(4)写出反应⑥的化学方程式__________________________________________________________________
(5)在上述① ~ ⑥反应中,属于取代反应的是______________,属于加成反应的是___________,
(6)写出E的结构简式:___________________________
(7)写出有机物 通过缩聚形成高分子聚酯F的结构简式:___________________________
通过缩聚形成高分子聚酯F的结构简式:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【有机化学基础】肉桂醛F (![]() )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
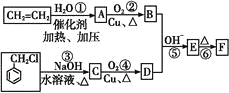
已知:两个醛分子在NaOH溶液作用下可以发生反应,生成一种羟基醛:
![]() +
+![]()
![]()
![]()
请回答:
(1)D的结构简式为 ;检验其中官能团的试剂为 。
(2)反应①~⑥中属于加成反应的是 (填序号)。
(3)写出有关反应③的化学方程式: 。
(4)在实验室里鉴定(![]() )分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是 (请按实验步骤操作的先后次序填写序号)。
)分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是 (请按实验步骤操作的先后次序填写序号)。
A.滴加AgNO3溶液 | B.加NaOH溶液 | C.加热 | D.用稀硝酸酸化 |
(5)下列关于E的说法正确的是 (填字母)。
a.能与银氨溶液反应 b.能与金属钠反应
c.1 mol E最多能和3 mol氢气反应 d.可以发生水解
(6)E的同分异构体有多种,其中之一甲符合条件:①苯环上只有一个取代基,②属于酯类,可由H和芳香酸G制得,现测得H分子的红外光谱和核磁共振氢谱如下图:(已知H的相对分子量为32)则甲的结构简式为
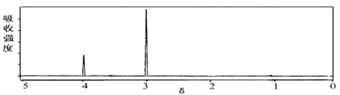
未知物H的核磁共振氢谱

未知物H的红外光谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,1-二环丙基乙烯(![]() )是重要医药中间体,下列关于该化合物的说法错误的是
)是重要医药中间体,下列关于该化合物的说法错误的是
A. 所有碳原子可能在同一平面B. 能使酸性高锰酸钾溶液褪色
C. 二氯代物有9种D. 生成1mol C8H18至少需要3mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题
学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理请回答下列问题:
(1)常温下,某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈 ______性,原因是________________;用离子方程式表示
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于 ______________;
(3)已知在H2S溶液中存在下列平衡: H2S![]() H++HS-
H++HS-
向H2S溶液中加入NaOH固体时,不考虑温度变化电离平衡向______移动,填“左”或“右”),c(H+)______。(填“增大”、“减小”或“不变”
向H2S溶液中加入NaHS固体时,电离平衡向______移动,填“左”或“右”)c(S2—)______。(填“增大”、“减小”或“不变”)

(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 ______ 填“A”或“B”;设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1______ m2。 (选填“![]() ”、“
”、“![]() ”、“
”、“![]() ”
”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成份CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3和ZnSO4溶液的一种工艺流程如下:
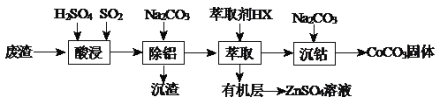
下表是相关金属离子生成氢氧化物沉淀的pH(按金属离子浓度为1.0mol·L-1计算):
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Co2+ | 7.6 | 9.4 |
Al3+ | 3.0 | 5.0 |
Zn2+ | 5.4 | 8.0 |
(1)写出“酸浸”时发生氧化还原反应的化学方程式________________________。
(2)“除铝”过程中需要调节溶液pH的范围为_________,形成沉渣时发生反应的离子方程式为______________________。
(3)在实验室里,萃取操作用到的玻璃仪器主要有_________________;上述“萃取”过程可表示为ZnSO4(水层)+2HX(有机层)![]() ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______________。
ZnX2(有机层)+H2SO4(水层),由有机层获取ZnSO4溶液的操作是______________。
(4)“沉钴”时,Na2CO3溶液滴加过快会导致产品不纯,请解释原因___________________。
(5)在空气中煅烧CoCO3生成某种钴氧化物和CO2,若充分煅烧一定量CoCO3后测定所得固体质量为2.41g,CO2的体积为0.672L(标准状况),假设固体为纯净物,其化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1mol·L-1的是( )
A.将0.1mol胆矾固体溶于100mL水中
B.将22.4LHCl气体溶于水配成1L溶液
C.将1L10mol·L-1的浓盐酸与9L水混合
D.10gNaOH固体溶解在水中配成250mL溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com