
科目:高中化学 来源: 题型:
(1)分析如图所示的四个装置,请回答下列问题:
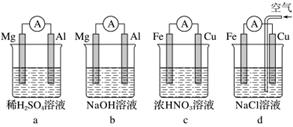
①装置a和b中铝电极上的电极反应式分别为________________________________________、________________________________________________________________________。
②装置c中产生气泡的电极为________电极(填“铁”或“铜”),装置d中铜电极上的电极反应式为____________________________________________________________。
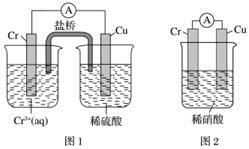
(2)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为_________________________________、________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应4NH3(g)+5 O2 (g)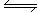 4NO (g)+6H2O (g)。回答下列问题:
4NO (g)+6H2O (g)。回答下列问题:
(1)在一定温度下,向一个5 L的密闭容器中充入0.20 mol的NH3和0.80 mol的O2,如反应初始6min内NH3的平均反应速率v(NH3)=0.003 mol·L-1·min-1,则6 min时c(O2)=___mol·L-1,NO的物质的量为________mol;反应一段时间后,达到平衡状态,如果这时向该密闭容器中再充入1 mol氩气,平衡时NH3的转化率________。(填“增大”“不变”或“减小”)
(2)判断该反应是否达到平衡的依据为________(填正确选项前的字母):a.体系压强不随时间改变 b.气体的密度不随时间改变 c.c(NH3)不随时间改变 d.单位时间里生成NO和H2O (g)的物质的量之比为4:6
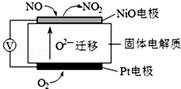 (3)氮的氧化物NOx是大气污染的主要污染物之一,通过NOx传感器可监测NOx的含量,其工作原理示意图如右:(工作原理和燃料电池类似)①Pt电极为 极(填正、负);NiO电极发生 反应(填“氧化”或“还原”).
(3)氮的氧化物NOx是大气污染的主要污染物之一,通过NOx传感器可监测NOx的含量,其工作原理示意图如右:(工作原理和燃料电池类似)①Pt电极为 极(填正、负);NiO电极发生 反应(填“氧化”或“还原”).
②写出NiO电极的电极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质与应用对应关系不正确的是
A.亚硫酸钠有还原性,可用作脱氧剂 B.FeCl3有氧化性,可用于制印刷电路
C.铝有还原性,可冶炼某些金属 D.浓硫酸有吸水性,可用于干燥氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
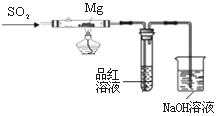 某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
实验Ⅰ 按右图所示进行实验。
(1)实验前需除去镁条表面氧化膜。用简易的物理
方法除氧化膜的操作是 ;
(2)实验室制取二氧化硫的化学方程式为 ;
(3)上述装置存在不合理之处,请提出1项改进建议 ;
 (4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
(4)实验时,先通入SO2直到 现象出现后,再点燃酒精灯;此操作目的是 。
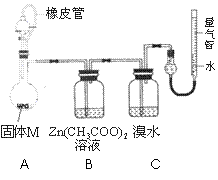
实验Ⅱ 确定固体M的成分。
实验装置如右图所示。将分液漏斗中稀硫酸(足量)
加入到烧瓶中,完全反应后,实验现象如下:
|
(5)实验时,B装置中反应的化学方程式为 ;
(6)已知镁的相对原子质量为24,则固体M中金属镁的质量为 g;实验前装置内有空气,对金属镁质量的测定结果的影响是 (填偏低、偏高、无影响);
(7)依以上实验,可确定固体M的成分有 种(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
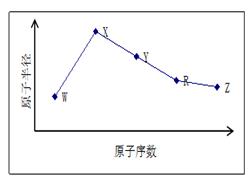
W、X、Y、Z、R是五种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10。X和Ne原子的核外电子数相差1。Y的最高价氧化物对应水化物是医用胃酸中和剂中的一种。R和W具有相同的最外层电子数。Z在同周期主族元素中原子半径最小。
(1)X是 ,Y是 。(填元素符号)
(2) 向新制的R的气态氢化物的饱和溶液中通入Z2的单质可以生成淡黄色沉淀,写出该反应的化学方程式 ,该实验事实证明,氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+)值增大,可以采取的措施是
A.加少量烧碱溶液 B.加蒸馏水
C.加少量醋酸钠固体 D.升高温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com