
| A. | H、D、T三种氢的核素在周期表中的位置不同 | |
| B. | 元素简单气态氢化物越稳定,则非金属性越强 | |
| C. | 核外电子层结构相同的离子,核电荷数越大其离子半径也越大 | |
| D. | ⅠA与ⅦA元素形成的化合物都是离子化合物 |
分析 A、三种核素质子数相同,在周期表占同一位置;
B、非金属性越强,氢化物越稳定;
C、核外电子层结构相同的离子,核电荷数越大半径越小;
D、ⅠA氢元素与ⅦA元素形成的化合物都是共价化合物.
解答 解:A、质子数相同,即原子序数相同,在周期表占同一位置,故A错误;
B、非金属性越强,氢化物越稳定,所以元素简单气态氢化物越稳定,则非金属性越强,故B正确;
C、核外电子层结构相同的离子,核电荷数越大半径越小,而不是越大,故C错误;
D、ⅠA氢元素与ⅦA元素形成的化合物都是共价化合物,不一定是离子化合物,故D错误;
故选B.
点评 本题考查原子结构与元素周期律知识,为高频考点,侧重于学生的分析能力的考查,注意把握元素周期律的递变规律以及比较角度,难度中等.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:解答题
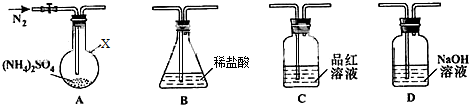
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
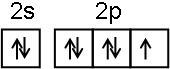 ;NF3中心原子轨道的杂化类型为sp3.
;NF3中心原子轨道的杂化类型为sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入Na2CO3溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | NH3通入AgNO3溶液中 | D. | SO2通入NaHS溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
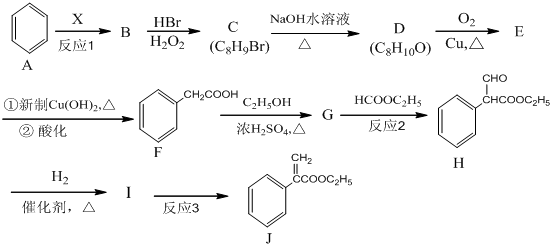
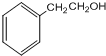 ,G的结构简式为
,G的结构简式为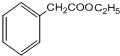 .
.

 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制0.1mol•L-1莫尔盐溶液500mL,需莫尔盐19.6克 | |
| B. | 可与含Fe2+、HClO、H+、Cl-微粒的溶液大量共存 | |
| C. | 加入过量Ba(OH)2溶液发生反应:2Ba2++2SO42-+Fe2++2OH-=2BaSO4↓+Fe(OH)2↓ | |
| D. | 取样,加入浓NaOH溶液并加热,出现可让蓝色石蕊试纸变红的气体,证明含NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO的电子式: | |
| B. | 16O的原子结构示意图: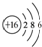 | |
| C. | 质子数为53,中子数为72的碘原子:53125I | |
| D. | 间羟基苯甲醛的结构简式: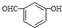 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 碳正离子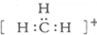 中质子数与电子数之比值为3:2 中质子数与电子数之比值为3:2 | |
| C. | 水合氢离子的结构式为  | |
| D. | NaHCO3水解反应的离子方程式:HCO3-+H2O?H3O++CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com