
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D、日常生活中无水乙醇常用于杀菌消毒 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、铝片与稀盐酸的反应 |
| B、Ba(OH)2?8H2O与NH4Cl的反应 |
| C、灼热的碳与二氧化碳的反应 |
| D、酒精在空气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用食醋清洗热水瓶中的水垢;用米汤检验碘盐中含有碘酸钾 |
| B、用小苏打可中和胃酸,热纯碱溶液可除油污.小苏打和纯碱可以用石灰水鉴别 |
| C、“84消毒液”和洁厕剂能同时使用,除污垢效果好 |
| D、用丁达尔效应区别鸡蛋白溶液和食盐水;用明矾可以净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液、胶体、浊液均为分散系,都属于混合物 |
| B、H2SO4、NaOH、NaC1均为强电解质,都属于离子化合物 |
| C、Al、Al2O3、Al(OH)3均能与盐酸反应又能与氢氧化钠溶液反应,都是具两性的化合物 |
| D、H2O、CH3COOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
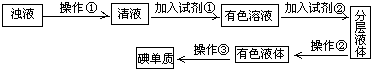
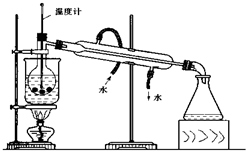
查看答案和解析>>
科目:高中化学 来源: 题型:
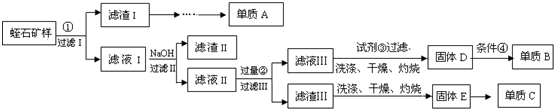
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取3.23 g NaCl固体 |
| B、称量NaOH固体时,应将砝码放在托盘天平右盘纸片上,NaOH固体放在左盘的纸片上 |
| C、用100 mL容量瓶配制50mL0.1 mol/L的盐酸 |
| D、稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水中,并不断搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com