
【题目】某实验小组用如图装置制备家用消毒液,并探究其性质.
(1)写出装有浓盐酸的仪器名称 , A中烧瓶内进行的反应中浓盐酸体现出的化学性质是
(2)写出装置B中发生的所有反应化学方程式
(3)装置c的作用是
反应停止后,各取洗气瓶中无色溶液5mL分别进行了如下实验:
操作 | 现象 |
A.测溶液pH,并向其中滴加2滴酚酞 | pH=13,溶液变红,5min后褪色 |
B. 向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(4)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去
为探究操作A中溶液褪色的原因,又补充了如下实验:
操作 | 现象 |
取 NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
获得结论:此实验小组制备的消毒液具有漂白性.
(5)操作B中溶液变成黄绿色的原因:(用离子方程式表示).
【答案】
(1)分液漏斗;酸性和还原性
(2)Cl2+2NaOH=NaCl+NaClO+H2O、HCl+NaOH=NaCl+H2O
(3)吸收多余氯气,避免污染空气
(4)5mL,pH=13
(5)2H++ClO﹣+Cl﹣═Cl2↑+H2O
【解析】解:(1)仪器A具有球形特征的漏斗且带有玻璃活塞,该仪器名称是分液漏斗;装置A:盐酸和二氧化锰在加热条件下反应4HCl+MnO2 ![]() Cl2↑+MnCl2+2H2O,氯化氢中氯元素的化合价由﹣1价→0价,作还原剂,氯化氢和二氧化锰反应生成氯化锰和水,体现酸性,所以盐酸的作用为酸性和还原性,所以答案是:分液漏斗;酸性和还原性;
Cl2↑+MnCl2+2H2O,氯化氢中氯元素的化合价由﹣1价→0价,作还原剂,氯化氢和二氧化锰反应生成氯化锰和水,体现酸性,所以盐酸的作用为酸性和还原性,所以答案是:分液漏斗;酸性和还原性;
(2.)氯化氢易挥发,在加热的条件下,部分氯化氢进入装置B与氢氧化钠发生中和反应,反应方程式为:HCl+NaOH=NaCl+H2O,主要反应为氯气和氢氧化钠反应:Cl2+2NaOH═NaClO+NaCl+H2O,制得消毒液,所以答案是:Cl2+2NaOH=NaCl+NaClO+H2O、HCl+NaOH=NaCl+H2O;
(3.)氯气有毒,为了防止多余的氯气污染空气,用NaOH溶液吸收,该反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,所以答案是:吸收多余氯气,避免污染空气;
(4.)酚酞在强碱性溶液中红色会褪去,但同样体积、同PH值的氢氧化钠溶液,滴加2滴酚酞溶液变红,30min后褪色,而消毒液,pH=13,溶液变红,5min后褪色,褪色时间短,说明此实验小组制备的消毒液具有漂白性,所以答案是:5mL,pH=13;
(5.)次氯酸根中氯为+1价,氯离子为﹣1价,在酸性条件下发生归中反应,生成氯气,反应为:2H++ClO﹣+Cl﹣═Cl2↑+H2O,黄绿色气体为氯气,所以答案是:2H++ClO﹣+Cl﹣═Cl2↑+H2O.


科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物V L(标准状况下),溶于m g水中,得到质量分数为w 的溶液,物质的量浓度为c mol/L,密度为d g/mL,则下列说法不正确的是( )
A.相对分子质量 M= ![]()
B.物质的量浓度 c= ![]()
C.溶质的质量分数 w= ![]()
D.溶液密度 d= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(HF)2(g)2HF(g),△H>0且平衡体系的总质量【m(总)】与总物质的量【n总】之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( ) 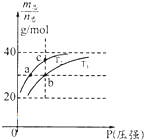
A.温度:T1<T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:Vb>Va
D.当 ![]() =30g/mol时,n(HF):n[(HF)2]=2:1
=30g/mol时,n(HF):n[(HF)2]=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护和治理环境是“十二五”规划中的一项重要内容,下列各项措施中,不利于改善环境质量的是( )
A.推行垃圾无害化与危险废弃物集中处理
B.大力推行洁净煤技术或改善能源结构
C.研制与提倡使用化学农药,以减少病虫害
D.积极推广使用无磷洗涤剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
(1)在25℃、101kPa时,16g CH4完全燃烧生成液态水时放出的热量是890.31kJ,则CH4燃烧的热化学方程式是 .
(2)已知:
C(s)+O2(g)═CO2(g);△H=﹣437.3kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(g);△H=﹣285.8kJmol﹣1
O2(g)═H2O(g);△H=﹣285.8kJmol﹣1
CO(g)+ ![]() O2(g)═CO2(g);△H=﹣283.0kJmol﹣1
O2(g)═CO2(g);△H=﹣283.0kJmol﹣1
则煤的气化主要反应的热化学方程式是:C(s)+H2O(g)═CO(g)+H2(g);△H=kJmol﹣1 , 该反应是(填“吸热”或者“放热”)反应,此法相比于传统的直接将煤中提取的C燃烧,你觉得可能的优点是什么? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入Y溶液中,生成沉淀的物质的量n2与所加X的物质的量n1的关系如图所示,符合图所示情况的是( )
A | B | C | D | |
X | NaOH | AlCl3 | HCl | NaAlO2 |
Y | AlCl3 | NaOH | NaAlO2 | HCl |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.2g Cu跟30.0mL 10.0molL﹣1的HNO3充分反应,还原产物有NO和NO2 , 若反应后溶液中有a mol H+ , 则此时溶液中含NO3﹣的物质的量为( )
A.0.5a mol
B.(0.1+a)mol
C.0.1a mol
D.2a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】你认为减少酸雨产生的途径可采取的措施是( )
①减少煤作燃料 ②造高工厂烟囱 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A. ①②③B. ②③④⑤C. ①③⑤D. ①③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com