
����Ŀ��I.��ҵ�����÷�ӦZnFe2 ��C2O4��3��6H2O![]() ZnFe2O4+2CO2��+4CO��+6H2O�Ʊ�ZnFe2O4��
ZnFe2O4+2CO2��+4CO��+6H2O�Ʊ�ZnFe2O4��
��1��ZnFe2O4��Fe�Ļ��ϼ�Ϊ___________��
��2���÷�Ӧ�л�ԭ������________���ѧʽ����ÿ����1mol ZnFe2O4��ת�Ƶĵ�����Ϊ________��
��.��pH=l��ij��ҺX�н�����NH4+��Al3+��Ba2+��Fe2+��Fe3+��CO32-��SO42-��Cl-��NO3-�е�һ�ֻ��֣�����ˮ�ĵ��뼰���ӵ�ˮ�⣩��ȡ����Һ��������ʵ�飬ʵ�������ͼ��
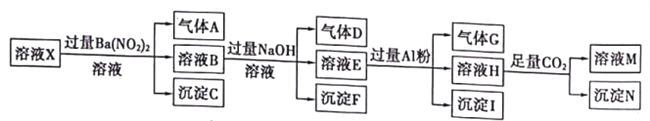
��֪��NO3-+Al+OH-+H2O��NH4++[Al��OH��4]-
��1����ҺX�г�H+�⣬һ�����ڵ�������_________________��
��2��д�����ɳ���N�����ӷ���ʽ_________________��
��3����ȡԭ��ҺX����ֱ�Ӽ���AgNO3��Һ������ɫ��������ȷ������Һ��һ������Cl-������Ϊ����˵���Ƿ������_______������������������������������____________��
���𰸡� +3 CO 4NA��2.408��1024 NH4+��Fe2+��SO42- Al��OH��4]-+ CO2=Al��OH��3��+HCO3- �� �������к���SO42-������AgNO3��Һ�����Ag2 SO4����ɫ�������ʲ���ȷ���Ƿ���Cl-
�������� I.��1��. ZnFe2O4��п�Ļ��ϼ�+2�ۣ���Ԫ�ػ��ϼ�-2�ۣ�����Ԫ�صĻ��ϼ�Ϊ+x�ۣ���ϻ��ϼ۴�����Ϊ0������õ�Fe�Ļ��ϼۣ�+2+x��2+��-2����4=0��x=+3���ʴ�Ϊ��+3��
��2��. ��ҵ�����÷�ӦZnFe2 ��C2O4��3��6H2O![]() ZnFe2O4+2CO2��+4CO��+6H2O�Ʊ�ZnFe2O4����Ӧ��������Ԫ�ػ��ϼ���+2�۱�Ϊ+3�ۣ�̼Ԫ�ػ��ϼ۴�+3�۱�Ϊ+4�ۺ�+2�ۣ���ԭ����Ϊ�� CO��ÿ����1mol ZnFe2O4��̼Ԫ�ػ��ϼ۴�+3�۱�Ϊ+2�������͵õ����ӣ����ݷ���ʽ��֪��ÿ����1mol ZnFe2O4��������4molCO��ת�Ƶ��ӵ����ʵ�����4mol��ת�Ƶĵ�������4NA��2.408��1024���ʴ��ǣ�CO��4NA��2.408��1024��
ZnFe2O4+2CO2��+4CO��+6H2O�Ʊ�ZnFe2O4����Ӧ��������Ԫ�ػ��ϼ���+2�۱�Ϊ+3�ۣ�̼Ԫ�ػ��ϼ۴�+3�۱�Ϊ+4�ۺ�+2�ۣ���ԭ����Ϊ�� CO��ÿ����1mol ZnFe2O4��̼Ԫ�ػ��ϼ۴�+3�۱�Ϊ+2�������͵õ����ӣ����ݷ���ʽ��֪��ÿ����1mol ZnFe2O4��������4molCO��ת�Ƶ��ӵ����ʵ�����4mol��ת�Ƶĵ�������4NA��2.408��1024���ʴ��ǣ�CO��4NA��2.408��1024��
��. pH=1����ҺΪǿ������Һ����ǿ������Һ��һ���������CO32-������������ᱵ���ɳ�������ó���CΪBaSO4��˵����Һ�к���SO42-����������A����Aֻ����NO��˵����Һ�к��л�ԭ�����ӣ���һ��ΪFe2+����ҺB�м������NaOH��Һ������Fֻ��ΪFe(OH)3����������D����DΪNH3��˵����Һ�к���NH4+����ҺE�м��������Al����������֪����ʽNO3-+Al+OH-+H2O��NH4++[Al��OH��4]-������ҺH�к���[Al��OH��4]-��ͨ��CO2���壬���ɳ���N����NΪAl��OH��3��˵����Һ�в�һ������Al3+���ӣ��ٸ������ӹ���֪ʶ����Һ�к���Fe2+���ӣ���һ������NO3-����һ������SO42-���ӣ���һ������Ba2+������ȷ���Ƿ��е�����Fe3+��Cl-���Դ˽��н����
��1��.��������������֪����ҺX�г���H+�⣬һ�����ڵ���������. NH4+��Fe2+��SO42-���ʴ��ǣ�. NH4+��Fe2+��SO42-��
��2��.��ҺH��ͨ������CO2������ҺH�е�[Al��OH��4]-��Ӧ����Al(OH)3��������Ӧ�����ӷ���ʽ�ǣ�Al��OH��4]-+ CO2=Al��OH��3��+HCO3-���ʴ��ǣ�Al��OH��4]-+ CO2=Al��OH��3��+HCO3-��
��3��. ȡԭ��ҺX����ֱ�Ӽ���AgNO3��Һ������ɫ����������ҺX��һ������SO42-������Ag����Ӧ����Ag2SO4����ɫ�������ʲ���ȷ��X��Һ���Ƿ���Cl�����ʴ��ǣ������������к���SO42-������AgNO3��Һ�����Ag2 SO4����ɫ�������ʲ���ȷ���Ƿ���Cl-��


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧ�����Һ��c(NH4��)=c(Cl-)����Ӧ����Һ��
A.����B.����C.����D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����װ���У���Һ�������Ϊ1 L��Ũ�Ⱦ�Ϊ0.1 mol��L��1������һ��ʱ���õ�·�о�ͨ����0.02 mol e���������������в���ȷ����
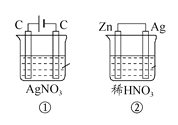
A. ��ͬ״���£������������������<��
B. ��ͨ��·ǰ��Һ��pH����>��
C. ��ͨ��·����Һ��pH����<��
D. ����������������>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ��ת��ͨ��һ����ѧ��Ӧ�ܹ�ʵ�ֵ���
A. Fe��Fe3O4 B. CuO��Cu(OH)2 C. NH3��NO2 D. SiO2��H2SiO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶�ʱ��1L�ܱ������з�����Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g) ��H=��196kJ/mol��������
2SO3(g) ��H=��196kJ/mol��������
��Ӧʱ��/min | n(SO2)/mol | n(O2)/mol |
0 | 2 | 1 |
5 | 1��2 | |
10 | 0��4 | |
15 | 0��8 |
����˵������ȷ����
A. ��Ӧ��ǰ5min��ƽ������Ϊv (SO2)=0��08mol��L1 min1
B. �����¶Ȳ��䣬��ƽ�����������ٳ���0��2molSO2��0��1molO2ʱ��v (��)�� v (��)
C. ���������������䣬����ʼʱ�������г���2molSO3����ƽ��ʱ����78��4kJ������
D. ��ͬ�¶��£���ʼʱ�������г���1��5mol SO3����ƽ��ʱSO3��ת����Ϊ40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��ȿ���Ũ�������ֿ��ù����������Ƹ������
A. Cl2 B. CO C. SO2 D. NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������NOCl�����л��ϳ�������Ҫ�Լ�������NO��Cl2�ڳ��³�ѹ�����Ե��¶ȣ��ºϳɣ����۵�-64.5�棬�е�-5.5�棬��ˮ��ˮ�⡣ʵ����ģ���Ʊ�װ����ͼ��ʾ�����ּг�װ��ʡ�ԣ���D��������ƿ����-10�����ˮ�С�
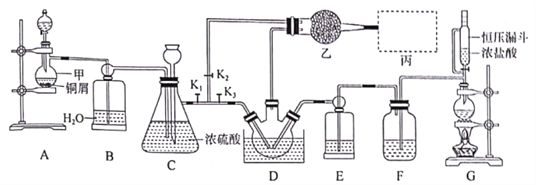
���������ϣ������������������
��NO2�۵�-64.5�棬�е�-5.5�棬�ɷ�����ӦCl2+2NO2=2NClO2
��NO��NaOH��Һ����Ӧ����NO2+NO+2NaOH =2NaNO2+H2O
��1��������������__________��
��2��ͼʾװ���к�ѹ©�����Һ©����ȣ����ŵ�Ϊ_________________��
��3��NOC1�����и�ԭ�Ӿ�����8�����ȶ��ṹ����NOCl�ĵ���ʽΪ_________��
��4��ʵ�鿪ʼʱ���ȴ�K1��K2���ر�K3����Һ©��������������ϡ���ᣬ��C�к���ɫ��ȫ��ʧ�ر�K1��K2����ʱװ��C������Ϊ_________ ����������Ũ���ᣬ��ȼ�ƾ��ƣ���______����װ�÷��ţ��г�������ɫ����ʱ����K1��K3���Ʊ�NOCl��
��5��װ������װ����ˮCaCl2��������Ϊ____________����Ϊβ������װ�ã������ѡ��Ϊ_________��

��6����ʵ�鿪ʼʱ���ȹر�K2����K1��K3 ��ʹNO��Cl2ֱ�ӷ�Ӧ�Ʊ�NOC1��������ʲô���________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 mol A��2 mol B����2 L�ܱ������з�����Ӧ2A(g) + B(g) ![]() 2C(g) ��H��0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����
2C(g) ��H��0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����
A��4 s�ڣ���(B)��0.075 mol/(L ��s)
B����c(A)�Uc(B)�Uc(C)��2�U1�U2 ʱ���÷�Ӧ���ﵽƽ��״̬
C���ﵽƽ��״̬����ֻ�����¶ȣ���C�����ʵ���Ũ������
D���ﵽƽ��״̬�����¶Ȳ��䣬��С�������������A��ת���ʽ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������к��е��������ʣ�������������NaOH��Һ����Һ���ķ�����ȥ����
A.�屽�е���B.���еı���
C.�����������D.�������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com